Varénicline - Varenicline
 | |
 | |
| Donnée clinique | |
|---|---|
| Appellations commerciales | Champix, Chantix, autres |
| AHFS / Drugs.com | Monographie |
| MedlinePlus | a606024 |
| Données de licence | |
Catégorie grossesse |
|
| Voies administratives |
Par la bouche |
| code ATC | |
| Statut légal | |
| Statut légal | |
| Données pharmacocinétiques | |
| Liaison protéique | <20 % |
| Métabolisme | Limité (<10 %) |
| Demi-vie d' élimination | 24 heures |
| Excrétion | Rein (81–92 %) |
| Identifiants | |
| |
| Numero CAS | |
| CID PubChem | |
| IUPHAR/BPS | |
| Banque de médicaments | |
| ChemSpider | |
| UNII | |
| KEGG | |
| ChEBI | |
| ChEMBL | |
| Tableau de bord CompTox ( EPA ) | |
| Données chimiques et physiques | |
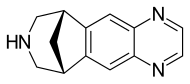
| Formule | C 13 H 13 N 3 |
| Masse molaire | 211,268 g·mol -1 |
| Modèle 3D ( JSmol ) | |
| |
| |
|
| |
La varénicline (nom commercial Chantix et Champix ) est un médicament utilisé pour le sevrage tabagique.
Les effets secondaires les plus courants sont les nausées (envie de vomir), l'insomnie (difficulté à dormir), les rêves anormaux, les maux de tête et la rhinopharyngite (inflammation du nez et de la gorge).
C'est un agoniste partiel de haute affinité pour le sous-type de récepteur nicotinique de l'acétylcholine α4β2 (nACh) qui conduit à la libération du neurotransmetteur dopamine dans le centre de récompense du noyau accumbens lorsqu'il est activé, et a donc la capacité de réduire les sentiments de envie et sevrage provoqués par l'arrêt du tabac . À cet égard, il est similaire à la cytisine et différent du bupropion antagoniste nicotinique et des thérapies de remplacement de la nicotine (TRN) comme les timbres et la gomme à la nicotine . On estime que la varénicline aide avec succès un fumeur sur onze à rester abstinent de tabac à six mois. Il figure sur la liste des médicaments essentiels de l'Organisation mondiale de la santé . Il est disponible sous forme de médicament générique.
Utilisations médicales
La varénicline est utilisée pour aider les personnes à arrêter de fumer ( arrêt du tabac ). Une méta-analyse a révélé que moins de 20 % des personnes traitées par la varénicline restent abstinentes de fumer à un an. Dans une méta-analyse de 2009 , la varénicline s'est avérée plus efficace que le bupropion ( rapport de cotes 1,40) et les thérapies de remplacement de la nicotine (TRN) (rapport de cotes 1,56).
Un aperçu Cochrane de 2013 et une méta-analyse du réseau ont conclu que la varénicline est le médicament le plus efficace pour le sevrage tabagique et que les fumeurs étaient près de trois fois plus susceptibles d'arrêter de fumer pendant qu'ils prenaient de la varénicline qu'avec un traitement placebo. La varénicline était plus efficace que le bupropion ou la TRN et aussi efficace que la TRN combinée pour le sevrage tabagique.
La varénicline n'a pas été testée chez les personnes de moins de 18 ans ou les femmes enceintes et son utilisation n'est donc pas recommandée par ces groupes. La varénicline est considérée comme un médicament de grossesse de classe C , car les études animales n'ont montré aucun risque accru d'anomalies congénitales ; cependant, aucune donnée d'études humaines n'est disponible. Une étude observationnelle est en cours pour évaluer les malformations liées à l'exposition à la varénicline, mais n'a pas encore de résultats. Un médicament alternatif est préféré pour le sevrage tabagique pendant l'allaitement en raison du manque d'information et sur la base des études animales sur la nicotine.
Effets secondaires
Des nausées légères sont l'effet secondaire le plus courant et sont observées chez environ 30 % des personnes prenant de la varénicline, bien que cela entraîne rarement (< 3 %) l'arrêt du médicament. D'autres effets secondaires moins courants incluent des maux de tête , des difficultés à dormir et des rêves intenses. Les effets secondaires rares rapportés par les personnes prenant de la varénicline par rapport au placebo incluent une modification du goût , des vomissements , des douleurs abdominales , des flatulences et de la constipation . Il a été estimé que pour cinq sujets prenant de la varénicline à des doses d'entretien, il y aurait un événement de nausée, et pour 24 et 35 sujets traités, il y aurait un événement de constipation et de flatulence, respectivement. Les effets secondaires gastro-intestinaux conduisent à l'arrêt du médicament chez 2 à 8 % des personnes utilisant la varénicline. L'incidence des nausées est dose-dépendante : l'incidence des nausées était plus élevée chez les personnes prenant une dose plus importante (30 %) par rapport au placebo (10 %) par rapport aux personnes prenant une dose plus faible (16 %) par rapport au placebo (11 %).
Dépression et suicide
En 2007, la FDA américaine avait annoncé avoir reçu des rapports post-commercialisation faisant état d' idées suicidaires et de comportements suicidaires occasionnels , de comportements erratiques et de somnolence chez les personnes utilisant la varénicline pour arrêter de fumer. En 2009, la FDA des États-Unis a exigé que la varénicline comporte un avertissement encadré indiquant que le médicament doit être arrêté si l'un de ces symptômes est ressenti.
Une revue systématique de 2014 n'a trouvé aucune preuve d'un risque accru de suicide . D'autres analyses sont parvenues à la même conclusion et n'ont trouvé aucun risque accru d'effets secondaires neuropsychiatriques avec la varénicline. Aucune preuve d'un risque accru d'événements cardiovasculaires, de dépression ou d'automutilation avec la varénicline par rapport à la thérapie de remplacement de la nicotine n'a été trouvée dans une étude de surveillance post-commercialisation.
En 2016, la FDA a supprimé l'avertissement de la boîte noire. Il est toujours conseillé aux gens d'arrêter le médicament s'ils "remarquent des effets secondaires sur l'humeur, le comportement ou la pensée".
Maladie cardiovasculaire
En juin 2011, la FDA des États-Unis a publié une annonce de sécurité selon laquelle la varénicline pourrait être associée à « un risque faible et accru de certains événements indésirables cardiovasculaires chez les personnes atteintes d'une maladie cardiovasculaire ».
Une revue antérieure de 2011 avait trouvé un risque accru d'événements cardiovasculaires par rapport au placebo. Les commentaires d'experts dans le même journal ont soulevé des doutes sur la méthodologie de l'examen, préoccupations qui ont été reprises par l' Agence européenne des médicaments et les examens ultérieurs. Les préoccupations particulières étaient « le faible nombre d'événements observés, les types d'événements comptés, le taux d'abandon plus élevé chez les personnes recevant un placebo, le manque d'informations sur le moment des événements et l'exclusion des études dans lesquelles personne n'avait un évènement."
En revanche, plusieurs revues systématiques et méta-analyses récentes n'ont trouvé aucune augmentation des événements cardiovasculaires indésirables globaux ou graves (y compris chez les personnes à risque de développer une maladie cardiovasculaire) associées à l'utilisation de la varénicline.
Mécanisme d'action
Varénicline affiche complet agonisme sur alpha 7 des récepteurs nicotiniques de l' acétylcholine et est un agoniste partiel sur le α 4 β 2 , α 3 β 4 , et α 6 β 2 sous - types. De plus, c'est un agoniste faible sur les récepteurs contenant α 3 β 2 .
L'agonisme partiel de la varénicline sur les récepteurs α 4 β 2 plutôt que l'agonisme total de la nicotine produit moins d'effet de libération de dopamine que celui de la nicotine. Cette liaison compétitive α 4 β 2 réduit la capacité de la nicotine à se lier et à stimuler le système dopaminergique mésolimbique, similaire au mode d'action de la buprénorphine dans le traitement de la dépendance aux opioïdes.
Pharmacocinétique
La majeure partie du composé actif est excrétée par les reins (92 à 93 %). Une faible proportion est glucuronidée , oxydée, N- formylée ou conjuguée à un hexose . La demi-vie d'élimination est d'environ 24 heures.
Histoire
L'utilisation de plantes Cytisus comme substituts du tabac pendant la Seconde Guerre mondiale a conduit à une utilisation comme aide au sevrage en Europe de l'Est et à l'extraction de la cytisine. Les analogues de la cytisine ont conduit à la varénicline chez Pfizer .
La varénicline a reçu un « examen prioritaire » par la FDA des États-Unis en février 2006, réduisant la période d'examen habituelle de dix mois à six mois en raison de son efficacité démontrée dans les essais cliniques et du manque perçu de problèmes de sécurité. L'approbation du médicament par l'agence est arrivée le 11 mai 2006. Le 29 septembre 2006, il a été approuvé pour la vente dans l' Union européenne .
Le 16 septembre 2021, Pfizer a annoncé le rappel de "tous les lots de son traitement anti-tabac, Chantix [Varenicline], en raison des niveaux élevés d'agents cancérigènes appelés nitrosamines dans les pilules". Cela faisait suite à une annonce du 2 juillet 2021 de la FDA selon laquelle elle « alertait les patients et les professionnels de la santé du rappel volontaire de Pfizer de neuf lots de médicaments pour le sevrage tabagique » et d'autres rappels par Pfizer les 19 juillet et 8 août. Le 24 juin , Pfizer avait suspendu la distribution de Chantix dans le monde entier ; "[l]'arrêt de la distribution [était] par prudence, dans l'attente de tests supplémentaires, a déclaré la société dans un e-mail. Selon le rapport annuel Pfizer Inc. 2020 Form 10-K, les produits à revenu élevé de la société comprennent[d] Chantix/Champix (varénicline) pour traiter la dépendance à la nicotine, [qui] a généré 919 millions de dollars de revenus en 2020.
Les références
Liens externes
- "Varénicline" . Portail d'information sur les médicaments . Bibliothèque nationale de médecine des États-Unis.
