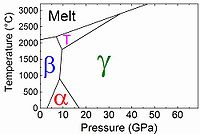
Allotropes du bore - Allotropes of boron
Le bore peut être préparé sous plusieurs formes cristallines et amorphes . Les formes cristallines bien connues sont le -rhomboédrique (α-R), le -rhomboédrique (β-R) et le -tétragonal (β-T). Dans des circonstances particulières, le bore peut également être synthétisé sous la forme de ses allotropes α-tétragonal (α-T) et γ-orthorhombique (γ) . Deux formes amorphes, l'une une poudre finement divisée et l'autre un solide vitreux, sont également connues. Bien qu'au moins 14 autres allotropes aient été signalés, ces autres formes sont basées sur des preuves ténues ou n'ont pas été confirmées expérimentalement, ou sont censées représenter des allotropes mixtes, ou des charpentes de bore stabilisées par des impuretés. Alors que la phase β-rhomboédrique est la plus stable et que les autres sont métastables, la vitesse de transformation est négligeable à température ambiante, et donc les cinq phases peuvent exister aux conditions ambiantes. Le bore en poudre amorphe et le bore β-rhomboédrique polycristallin sont les formes les plus courantes. Ce dernier allotrope est un matériau gris très dur, environ dix pour cent plus léger que l'aluminium et avec un point de fusion (2080 °C) plusieurs centaines de degrés plus élevé que celui de l'acier.
Le bore élémentaire a été trouvé dans la poussière d'étoiles et les météorites, mais n'existe pas dans l'environnement à haute teneur en oxygène de la Terre. Il est difficile à extraire de ses composés. Les premières méthodes impliquaient la réduction de l'oxyde borique avec des métaux tels que le magnésium ou l' aluminium . Cependant, le produit est presque toujours contaminé par des borures métalliques . Le bore pur peut être préparé en réduisant les halogénures de bore volatils avec de l' hydrogène à haute température. Le bore très pur, destiné à être utilisé dans l'industrie des semi-conducteurs, est produit par la décomposition du diborane à haute température, suivie d'une purification par fusion de zone ou par le procédé Czochralski . Les monocristaux de phases de bore pur sont encore plus difficiles à préparer , en raison du polymorphisme et de la tendance du bore à réagir avec les impuretés ; la taille typique des cristaux est d'environ 0,1 mm.
Résumé des propriétés
| Phase de bore | -R | -T | -R | -T | ?? | Amorphe | |
|---|---|---|---|---|---|---|---|
|
|
|
||||||
| Symétrie | Rhomboédrique | tétragonale | Rhomboédrique | tétragonale | orthorhombique | Semi-aléatoire | Semi-aléatoire |
| Occurrence | commun | spécial | commun | commun | spécial | ||
| Atomes/cellule unitaire | 12 | 50 | 105‒108 | 192 | 28 | ||
| Densité (g/cm 3 ) | 2,46 | 2.29‒2.39 | 2,35 | 2,36 | 2,52 | 1,73 | 2,34–35 |
| Dureté Vickers (GPa) | 42 | 45 | 50-58 | ||||
| Module de vrac (GPa) | 224 | 184 | 227 | ||||
| Bande interdite (eV) | 2 | 1.6 | ~2.6 | 2.1 | 0,56-0,71 | ||
| Couleur | Les cristaux sont rouge clair | Noir et opaque, avec un lustre métallique | Gris argenté foncé à brillant | Noir rouge | Gris foncé | Noir à brun | Noir opaque |
| Année du premier rapport | 1958 | 1943/1973 | 1957 | 1960 | 2009 | 1808 | 1911 |
Bore -rhomboédrique
Le bore -rhomboédrique a une maille élémentaire de douze atomes de bore. La structure se compose de B
12icosaèdre dans lequel chaque atome de bore a cinq voisins les plus proches au sein de l'icosaèdre. Si la liaison était du type covalent conventionnel, chaque bore aurait donné cinq électrons. Cependant, le bore n'a que trois électrons de valence, et on pense que la liaison dans le B
12 Les icosaèdres sont obtenus par les liaisons dites déficientes en électrons à 3 centres où la charge électronique s'accumule au centre d'un triangle formé de trois atomes adjacents.
Le B isolé
12les icosaèdres ne sont pas stables, en raison de la non-uniformité du nid d'abeilles ; ainsi le bore n'est pas un solide moléculaire, mais les icosaèdres qu'il contient sont reliés par de fortes liaisons covalentes.
bore -tétragonal
Le α-tétragonal pur ne peut être synthétisé que sous forme de couches minces déposées sur un substrat sous-jacent de carbure de bore isotrope (B 50 C 2 ) ou de nitrure (B 50 N 2 ). La plupart des exemples de bore α-tétragonal sont en fait des carbures ou des nitrures riches en bore .
Bore -rhomboédrique
Le bore β-rhomboédrique a une maille élémentaire contenant 105 à 108 (idéalement exactement 105) atomes. La plupart des atomes forment des icosaèdres discrets B 12 ; quelques-uns forment des icosaèdres partiellement interpénétrés, et il y a deux unités deltaédriques B 10 et un seul atome B central. Pendant longtemps, il n'a pas été clair si la phase ou est la plus stable aux conditions ambiantes ; cependant, un consensus s'est progressivement dégagé sur le fait que la phase est l'allotrope le plus thermodynamiquement stable.
bore -tétragonal
La phase a été produite en 1960 par réduction à l'hydrogène de BBr 3 sur des filaments de tungstène , de rhénium ou de tantale chauds à des températures de 1270-1550 °C (c'est-à-dire dépôt chimique en phase vapeur ). D'autres études ont reproduit la synthèse et confirmé l'absence d'impuretés dans cette phase.
γ-bore
La phase peut être décrite comme un arrangement de type NaCl de deux types d'amas, les icosaèdres B 12 et les paires B 2 . Il peut être produit en comprimant d'autres phases de bore à 12-20 GPa et en chauffant à 1500-1800 °C, et reste stable aux conditions ambiantes. Il existe des preuves d'un transfert de charge significatif des paires B 2 vers les icosaèdres B 12 dans cette structure ; en particulier, la dynamique du réseau suggère la présence d'interactions électrostatiques significatives à longue distance.
Cette phase a été rapportée par Wentorf en 1965 ; cependant, ni la structure ni la composition chimique n'ont été établies. La structure a été résolue à l'aide de calculs de prédiction de structure cristalline ab initio et confirmée à l'aide de la diffraction des rayons X sur monocristal .
Bore cubique
Sullenger et al. (1969) et McConville et al. (1976) ont rapporté un allotrope cubique de bore, obtenu dans des expériences de plasma d'argon, avec une maille unitaire de 1705 ± 3 atomes et une densité de 2,367 g/cm 3 . Bien que cet allotrope soit parfois mentionné dans la littérature, aucun travail ultérieur ne semble avoir été publié pour confirmer ou discréditer son existence. Donohue (1982) a fait remarquer que le nombre d'atomes dans la cellule unitaire ne semblait pas être lié à l'icosaèdre (l'icosaèdre étant un motif commun aux structures de bore).
Phase supraconductrice haute pression
La compression du bore au-dessus de 160 GPa produit une phase de bore avec une structure encore inconnue. Contrairement aux autres phases, qui sont des semi - conducteurs , cette phase est un métal et devient un supraconducteur avec une température critique passant de 6 K à 160 GPa à 11 K à 250 GPa. Cette transformation structurelle se produit à des pressions auxquelles la théorie prédit que les icosaèdres se dissocieront. La spéculation quant à la structure de cette phase a inclus le cubique à faces centrées (analogue à Al) ; -Ga et tétragonal centré sur le corps (analogue à In). Il a également été suggéré que la transition non métal-métal est simplement le résultat d'une fermeture de bande interdite , comme cela se produit avec l'iode, plutôt que d'une transition structurelle.
Borophène
Il existe plusieurs formes bidimensionnelles de bore (appelées ensemble borophènes ), et encore plus sont prédites théoriquement.
Borosphère
La découverte de la molécule allotropique quasi sphérique borosphèrene (B 40 ) a été annoncée en juillet 2014.
Bore amorphe
Le bore amorphe contient des icosaèdres réguliers B 12 qui sont liés de manière aléatoire les uns aux autres sans ordre à longue distance. Le bore amorphe pur peut être produit par décomposition thermique du diborane à des températures inférieures à 1000 °C. Le recuit à 1000 °C convertit le bore amorphe en bore -rhomboédrique. Des nanofils de bore amorphe (30 à 60 nm d'épaisseur) ou des fibres peuvent être produits par pulvérisation cathodique magnétron et dépôt chimique en phase vapeur assisté par laser , respectivement ; et ils se convertissent également en nanofils de bore -rhomboédriques lors d'un recuit à 1000 °C.
Remarques
Les références
Bibliographie
- Amberger, E. (1981). "Le bore élémentaire". Dans Buschbeck, KC (éd.). Manuel Gmelin de chimie inorganique et organométallique : B Boron, Supplément 2 (8e éd.). Berlin : Springer-Verlag. p. 1-112. ISBN 3-540-93448-0.
- Donohue, J. (1982). Les structures des éléments . Malabar, Floride : Robert E. Krieger. ISBN 0-89874-230-7.
- Housecroft, CE ; Sharpe, AG (2008). Chimie inorganique (3e éd.). Harlow : Pearson Education. ISBN 978-0-13-175553-6.
- Madelung, O. (1983). Données numériques de Landolt-Bornstein et relations fonctionnelles en science et technologie. Nouvelle série. Groupe III. Tome 17 : Semi-conducteurs. Sous-volume e : Physique des éléments non tétraédriques et des composés binaires I . Springer-Verlag : New York. ISBN 0-387-11780-6.
- Nelmes, RJ; Jour d'amour, JS; Allan, DR ; Besson, JM ; Hamel, G. ; Grima, P.; Hull, S. (1993). « Mesures de diffraction des neutrons et des rayons X du module de masse du bore ». Examen physique B . 47 (13) : 7668-7673. Bibcode : 1993PhRvB..47.7668N . doi : 10.1103/PhysRevB.47.7668 . PMID 10004773 .
- Oganov, AR ; Chen, J.; Peut.; Verre, CW ; Yu, Z. ; Kurakevych, OO ; Solozhenko, VL (12 février 2009). « Forme ionique à haute pression de bore élémentaire ». Nature . 457 (7027) : 863-868. arXiv : 0911.3192 . Bibcode : 2009Natur.457..863O . doi : 10.1038/nature07736 . PMID 19182772 .
- Sullenger, DB ; Phipps, KD ; Seabaugh, PW ; Hudgens, CR ; Sables, DE; Cantrell, JS (1969). « Modifications du bore produites dans un plasma d'argon couplé par induction ». Sciences . 163 (3870): 935‒937. Bibcode : 1969Sci ... 163..935S . doi : 10.1126/science.163.3870.935 . PMID 17737317 .
- Talley, CP; La Plaça, S.; Post, B. (1960). "Un nouveau polymorphe du bore" . Acta Crystallographica . 13 (3) : 271‒2. doi : 10.1107/S0365110X600000613 .
- Wang, YQ; Duan, XF (2003). "Nanofils de bore cristallins". Lettres de Physique Appliquée . 82 (2): 272. bibcode : 2003ApPhL..82..272W . doi : 10.1063/1.1536269 . S2CID 122278136 .
- Wentorf, RH (1965). "Bore : Une autre forme". Sciences . 147 (3653) : 49-50. Bibcode : 1965Sci ... 147 ... 49W . doi : 10.1126/science.147.3653.49 . PMID 17799779 .
- Wiberg, N. (2001). Chimie inorganique . San Diego : Presse académique. ISBN 0-12-352651-5.
- Will, G.; Kiefer, B. (2001). « Densité de déformation électronique dans le -bore rhomboédrique ». Zeitschrift für anorganische und allgemeine Chemie . 627 (9) : 2100‒104. doi : 10.1002/1521-3749(200109)627:9<2100::AID-ZAAC2100>3.0.CO;2-G .
- Zarecnaya, EY ; Dubrovinsky, L.; Dubrovinskaia, N.; Filinchuk, Y.; Chernychov, D.; Dmitriev, V. ; Miyajima, N.; El Goresy, A.; et al. (2009). « Phase de haute pression optiquement transparente semi-conductrice super dure de bore ». Lettres d'examen physique . 102 (18) : 185501‒4. Bibcode : 2009PhRvL.102r5501Z . doi : 10.1103/PhysRevLett.102.185501 . PMID 19518885 . S2CID 14942345 .
Liens externes
-
 Médias liés aux allotropes du bore sur Wikimedia Commons
Médias liés aux allotropes du bore sur Wikimedia Commons