Oxyde d'amine - Amine oxide
Un oxyde d'amine , également connu sous le nom d' amine N -oxyde et N -oxyde , est un composé chimique qui contient le groupe fonctionnel R 3 N + −O − , une liaison covalente coordonnée N−O avec trois côtés hydrogène et/ou hydrocarbure supplémentaires chaînes attachées à N. Parfois, il est écrit comme R 3 N→O ou, à tort, comme R 3 N=O.
Au sens strict, le terme oxyde d'amine ne s'applique qu'aux oxydes d' amines tertiaires . Parfois, il est également utilisé pour les dérivés analogues d'amines primaires et secondaires.
Des exemples d'oxydes d'aminés comprennent la pyridine N -oxyde , un solide cristallin soluble dans l'eau avec un point de fusion 62-67 ° C, et N de N de -oxyde , qui est un oxydant.
Applications
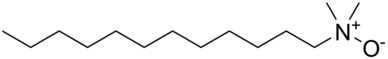
Les oxydes d'amine sont des tensioactifs couramment utilisés dans les produits de consommation tels que les shampooings, les revitalisants, les détergents et les nettoyants pour surfaces dures. L'oxyde d'alkyldiméthylamine (longueurs de chaîne C10-C16) est l'oxyde d'amine le plus utilisé dans le commerce. Ils sont considérés comme une classe de composés à haut volume de production dans plus d'un pays membre de l' Organisation de coopération et de développement économiques (OCDE) ; avec une production annuelle de plus de 26 000, 16 000 et 6 800 tonnes (28 700, 17 600 et 7 500 tonnes courtes) aux États-Unis, en Europe et au Japon, respectivement. En Amérique du Nord, plus de 95 % des oxydes d'amines sont utilisés dans les produits d'entretien ménager. Ils servent de stabilisants, d'épaississants, d'émollients, d'émulsifiants et de conditionneurs avec des concentrations actives comprises entre 0,1 et 10 %. Le reste (< 5%) est utilisé dans les produits de soins personnels, institutionnels, commerciaux et pour des utilisations brevetées uniques telles que la photographie.
Propriétés
Les oxydes d'amines sont utilisés comme groupe protecteur pour les amines et comme intermédiaires chimiques . Les oxydes d' alkylamine à longue chaîne sont utilisés comme tensioactifs amphotères et stabilisants de mousse .
Les oxydes d'amines sont des molécules très polaires et ont une polarité proche de celle des sels d'ammonium quaternaire . Les petits oxydes d'amines sont très hydrophiles et ont une excellente solubilité dans l' eau et une très mauvaise solubilité dans la plupart des solvants organiques .
Les oxydes d'amines sont des bases faibles avec un p K b d'environ 4,5 qui forment R 3 N + -OH, des hydroxylamines cationiques , lors de la protonation à un pH inférieur à leur p K b .
Synthèse
Presque tous les oxydes d'amines sont préparés par oxydation d'amines aliphatiques tertiaires ou de N- hétérocycles aromatiques . Le peroxyde d'hydrogène est le réactif le plus courant à la fois dans l'industrie et dans le milieu universitaire, mais les peracides sont également importants. Des agents oxydants plus spécialisés peuvent voir une utilisation de niche, par exemple l'acide de Caro ou le m CPBA . Les réactions spontanées ou catalysées utilisant l'oxygène moléculaire sont rares. Certaines autres réactions produiront également des oxydes d'amines, comme l' élimination rétro-Cope , mais elles sont rarement employées.
Réactions
Les oxydes d'amine présentent de nombreux types de réactions.
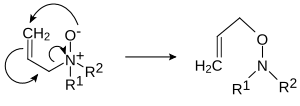
- Elimination pyrolytique. Les oxydes d'amine, lorsqu'ils sont chauffés à 150-200 °C, éliminent une hydroxylamine, ce qui donne un alcène . Cette réaction de synélimination pyrolytique est connue sous le nom de réaction de Cope . Le mécanisme est similaire à celui de l' élimination de Hofmann .
- Réduction aux amines. Les oxydes d'amine sont facilement convertis en l'amine mère par des réactifs de réduction courants, notamment l'hydrure de lithium et d'aluminium , le borohydrure de sodium , la réduction catalytique , le zinc / acide acétique et le fer/acide acétique. Les N- oxydes de pyridine peuvent être désoxygénés par l'oxychlorure de phosphore
- Catalyse sacrificielle. Les oxydants peuvent être régénérés par réduction des N- oxydes, comme dans le cas de la régénération du tétroxyde d'osmium par le N- méthylmorpholine N- oxyde.
- O- alkylation. Les N- oxydes de pyridine réagissent avec les halogénures d'alkyle en un produit O- alkylé
- Bis- ter les dérivés -pyridine adsorbées sur des surfaces d'argent sont discutées à réagir avec l' oxygène de bis- ter -pyridine N -oxyde. Cette réaction peut être suivie par microscopie à effet tunnel à balayage vidéo avec une résolution sous-moléculaire.
- Dans le réarrangement de Meisenheimer (d'après Jakob Meisenheimer ) certains N -oxydes R 1 R 2 R 3 N + O − se réarrangent en hydroxylamines R 2 R 3 N−O−R 1
- Dans la réaction de Polonovski, un N- oxyde tertiaire est clivé par l'anhydride d'acide acétique en l' acétamide et l' aldéhyde correspondants :
Métabolites
Les oxydes d'amines sont des métabolites courants des médicaments et des substances psychoactives . Les exemples incluent la nicotine , le zolmitriptan et la morphine .
Les oxydes d'amine de médicaments anticancéreux ont été développés en tant que promédicaments qui sont métabolisés dans le tissu cancéreux déficient en oxygène en le médicament actif.
Sécurité humaine
Les oxydes d'amine (AO) ne sont pas connus pour être cancérigènes, sensibilisants cutanés ou provoquer une toxicité pour la reproduction. Ils sont facilement métabolisés et excrétés en cas d'ingestion. L'ingestion chronique par les lapins a révélé une diminution du poids corporel, de la diarrhée et des opacités lenticulaires à des niveaux d'effets nocifs observés (LOAEL) les plus faibles, compris entre 87 et 150 mg AO/kw pc/jour. Des tests d'exposition cutanée humaine ont montré qu'après 8 heures, moins de 1% est absorbé dans le corps. L'irritation des yeux due aux oxydes d'amines et autres tensioactifs est modérée et temporaire sans effets durables.
Sécurité environnementale
Les oxydes d'amine avec une longueur de chaîne moyenne de 12,6 ont été mesurés pour être solubles dans l'eau à ~ 410 g L -1 . Ils sont considérés comme ayant un faible potentiel de bioaccumulation chez les espèces aquatiques d'après les données de log K oe provenant de longueurs de chaîne inférieures à C14 (facteur de bioconcentration < 87 %). Les niveaux d'AO dans les affluents non traités se sont avérés être de 2,3 à 27,8 ug L -1 , tandis que dans les effluents, ils se sont avérés être de 0,4 à 2,91 ug L -1 . Les concentrations d'effluents les plus élevées ont été trouvées dans les stations d'épuration par fossés d'oxydation et filtres ruisselants. En moyenne, plus de 96 % d'élimination a été trouvée avec le traitement secondaire des boues activées. La toxicité aiguë chez les poissons, telle qu'indiquée par les tests LC50 96h, est de l'ordre de 1 000 à 3 000 ug L -1 pour des longueurs de chaîne carbonée inférieures à C14. Les valeurs de CL50 pour des longueurs de chaîne supérieures à C14 vont de 600 à 1400 ug L -1 . Les données de toxicité chronique pour les poissons sont de 420 ug/L. Lorsqu'elle est normalisée à C12.9, la CSEO est de 310 ug L −1 pour la croissance et l'éclosabilité.
Voir également
- Groupe fonctionnel
- Amine , NR 3
- Hydroxylamine , NR 2 OH
- Oxyde de phosphine , PR 3 =O
- Sulfoxyde , R 2 S=O
- Azoxy , RN=N + (O − )R RN=N + RO −
- Groupe aminoxyle Radicaux de structure générale R 2 N–O•
- Catégorie:Oxydes d'amine , contenant tous les articles sur des composés d'oxyde d'amine spécifiques