Amitraze - Amitraz
|
|

|
|
| Noms | |
|---|---|
|
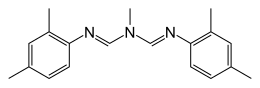
Nom IUPAC
N , N' -[(Méthylimino)diméthylidyne]di-2,4-xylidine
|
|
| Identifiants | |
|
Modèle 3D ( JSmol )
|
|
| ChEBI | |
| ChEMBL | |
| ChemSpider | |
| Carte d'information de l'ECHA |
100.046.691 |
| KEGG | |
|
CID PubChem
|
|
| UNII | |
|
Tableau de bord CompTox ( EPA )
|
|
|
|
|
|
| Propriétés | |
| C 19 H 23 N 3 | |
| Masse molaire | 293,41 g/mol |
| Point de fusion | 86 à 87 °C (187 à 189 °F ; 359 à 360 K) |
| Insoluble | |
| La pression de vapeur | 2,6 x 10 −6 mmHg |
| Pharmacologie | |
| QP53AD01 ( OMS ) | |
|
Sauf indication contraire, les données sont données pour les matériaux dans leur état standard (à 25 °C [77 °F], 100 kPa). |
|
|
|
|
| Références de l'infobox | |
L'amitraze (code de développement BTS27419) est un acaricide et insecticide non systémique et a également été décrit comme un scabicide . Il a été synthétisé pour la première fois par Boots Co. en Angleterre en 1969. L'amitraze s'est avéré avoir un effet répulsif contre les insectes, agit comme insecticide et également comme synergiste de pesticides . Son efficacité repose sur l' activité agoniste alpha-adrénergique , l'interaction avec les récepteurs octopamine du système nerveux central et l'inhibition des monoamine oxydases et de la synthèse des prostaglandines . Par conséquent, elle conduit à une surexcitation et par conséquent à une paralysie et à la mort chez les insectes. Parce que l'amitraze est moins nocif pour les mammifères, l'amitraze est parmi de nombreux autres usages mieux connus comme insecticide contre l'infestation par les acariens ou les tiques des chiens. Il est également largement utilisé dans l'industrie apicole comme moyen de lutte contre l' acarien Varroa destructor , bien qu'il y ait eu des rapports récents de résistance (en raison d'une surutilisation et d'une utilisation non indiquée sur l'étiquette).
Utilisation
L'amitraze est particulièrement efficace contre les acariens , mais il est utilisé comme pesticide dans de nombreux domaines différents. Par conséquent, l'amitraze est disponible sous de nombreuses formes différentes, telles qu'une poudre mouillable, un concentré émulsifiable, un concentré/liquide soluble et un collier imprégné (pour les chiens). Il est caractérisé comme un insectifuge, un insecticide et un synergiste de pesticides . Ce sont les propriétés qui le rendent particulièrement utile comme pesticide :
- L'effet répulsif fait que les insectes se détournent de leur cible car celle-ci est traitée avec de l'amitraze.
- Il agit comme un insecticide , ce qui signifie qu'il peut être utilisé pour lutter contre les insectes nuisibles directement ou indirectement à l'homme.
- En tant que synergiste de pesticides, il augmente également l'effet de certains autres pesticides s'ils sont combinés avec de l'amitraze.
Ceux-ci peuvent être retracés aux mécanismes d'action, qui conduisent à un large champ d'effets, y compris la létalité directe , les effets comportementaux excitants-répulsifs et la chimiostérilisation pour l'espèce cible. De plus, il cause généralement de faibles dommages aux espèces non ciblées, ce qui est l'un des avantages de l'amitraze. De plus, l'amitraze est particulièrement efficace contre les insectes tels que les tétranyques et les tiques dans leurs formes juvéniles et résistantes. À des fins agricoles, l'amitraze est principalement utilisée pour lutter contre le psylle du poirier (Cacopsylla pyricola) sur les cultures de poiriers de l'Oregon et les aleurodes et les acariens sur les cultures de coton ou de poirier. Il est également appliqué sur les fruits à pépins, les agrumes, le coton, les fruits à noyau, les fruits de brousse, les fraises, le houblon, les cucurbitacées, les aubergines, les poivrons, les tomates et les plantes ornementales pour contrôler toutes les étapes des acariens tétranychides et ériophyides, des drageons de poire, des cochenilles , des cochenilles , aleurodes , pucerons et œufs et larves de premier stade des lépidoptères . Pour appliquer l'amitraz, diverses techniques peuvent être utilisées telles qu'un jet d'air et de concentré sur les poires ou par rampe au sol et par avion sur le coton. Les différences territoriales dans l'utilisation de l'amitraze dépendent des espèces d'acariens qui infestent les cultures/arbres/etc., la pratique locale, et le nombre et la taille des poiriers. Une infestation par exemple par Tetranychus spp nécessite des taux plus élevés d'amitraze. Compte tenu de ces facteurs, les volumes d'application d'amitraze ont été normalisés en termes de concentration maximale de pulvérisation et de taux d'amitraze par hectare.
Outre son application comme pesticide sur les plantes, l'amitraze est également utilisé comme ectoparasiticide animal sur les bovins, les chèvres, les moutons, les porcs et les chiens. Dans ces applications, il est exclusivement appliqué à l'extérieur. Il atteint une efficacité particulière contre les acariens (d'abord Demodex canis ), mais il agit également contre les poux , les mouches et tous les stades de développement des tiques . En combinaison avec des agents supplémentaires, il peut également être utilisé contre les infestations de puces. Pour le traitement des chiens, l'amitraze est disponible sous forme de collier ou de solution de pulvérisation ou de lavage et a un effet immédiat contre les infestations de tiques ainsi qu'un effet préventif. Dans certains pays, les émulsions d'amitraze sont également appliquées pour traiter la démodécie des chats ou des chiens, une infestation excessive d'acariens de la famille des Demodicidae. Pour le traitement des bovins, des moutons, des chèvres et des porcs, l'amitraze est disponible sous forme de solution de pulvérisation ou de lavage, pour traiter ou prévenir les infestations par les acariens, les poux, les mouches et les tiques. Ainsi, les porcs et les bovins doivent être pulvérisés et les moutons et les chèvres doivent être lavés. D'autres espèces animales - les chevaux ou les chihuahuas, par exemple - ne doivent pas être traitées avec de l'amitraze car des effets indésirables peuvent survenir.
Effets indésirables
Les effets indésirables chez les mammifères sont causés par l'activité agoniste alpha-adrénergique de l'amitraz. Les symptômes peuvent inclure une pression artérielle et un pouls faibles, une hypothermie, une léthargie, une absence d'appétit, des vomissements, une augmentation de la glycémie et des problèmes digestifs. De plus, des irritations de la peau ou des muqueuses peuvent survenir chez les chiens en réponse à un collier contenant de l'amitraze. Cela peut entraîner des démangeaisons, un eczéma, une alopécie ou une conjonctivite .
Toxicité
Toxicité humaine
En 2006, l'Environmental Protection Agency ( USEPA ) des États-Unis a réévalué la classification de l'amitraze en un descripteur non quantifiable de « preuves suggestives de cancérogénicité » et, en 2013, a déterminé que la quantification du risque à l'aide d'une approche non linéaire pour l'amitraze tiendrait compte de manière adéquate pour toute toxicité chronique, y compris la cancérogénicité, qui pourrait résulter d'une exposition à l'amitraze et à ses métabolites. L'exposition accidentelle des hommes à de plus grandes quantités d'amitraze peut entraîner la mort par insuffisance respiratoire, principalement après absorption orale ou inhalation. En Turquie en 1989, 41 cas d'intoxications mortelles à l'amitraze ont été détectés. La dose toxique observée chez environ 50 % de ces patients a été de 0,3 g à 1,25 g de formulations d'amitraze à 12,5 % et de 0,5 à 2 g de formulations à 20 %. Les autres patients ont pris des doses allant jusqu'à 10 g. Les autres symptômes fréquents après une intoxication massive à l'amitraze sont la dépression du SNC , la dépression respiratoire , le myosis , l' hypothermie , l' hyperglycémie , la perte de conscience , les vomissements et la bradycardie .
Traitement
En cas de surdosage d'amitraz chez l'homme, l' atipamézole ou la yohimbine , qui agissent comme des antagonistes α2 peuvent être utilisés comme antidote. Initialement, il est important de retirer le patient de la zone contaminée par l'amitraze. Lorsque l'amitraze a été inhalé, le patient doit d'abord recevoir une protection respiratoire. De plus, le patient doit recevoir 4 L d'oxygène par minute. En cas d'intoxication par contact cutané, les vêtements contaminés doivent être retirés en premier. Les zones touchées doivent être lavées à l'eau. Si les yeux ont été exposés à l'amitraz, une anesthésie doit être administrée et les yeux soigneusement lavés. Après la prise orale d'amitraz, il est important de faire boire au patient env. 0,3 L d'eau pour réduire l'effet irritant de l'amitraz sur l'œsophage. De plus, il est important d'empêcher autant que possible le patient de vomir, afin de réduire le risque d'aspiration supplémentaire d'amitraze. Par la suite, le patient doit être observé pendant au moins 24 heures pour s'assurer que les symptômes ne se reproduisent pas.
Toxicité non humaine
| Espèce | Mode d'administration | Dose |
|---|---|---|
| Rat | oral | 400 mg/kg |
| dermique | >1600 mg/kg | |
| intrapéritonéale | 800 mg/kg | |
| Souris | oral | 1600 mg/kg |
| intrapéritonéale | >100mg/kg | |
| Lapin | oral | >100mg/kg |
| dermique | >200 mg/kg | |
| Babouin | oral | 150-250 mg/kg |
| Chien | oral | 100 mg/kg |
| Cochon d'Inde | oral | 400 à 800 mg/kg |
Synthèse
Depuis sa découverte par Boots Co. en 1969, trois voies de synthèse principales pour l'amitraze ont été développées, qui se distinguent en termes de facilité et de généralité.
Voie 1 : 2,4-Xylidine + orthoformate de triéthyle + méthylamine (formation d'imine/formation d'amine) :
L'une des premières usines de fabrication d'amitraze a utilisé ce schéma réactionnel (figure 1). Par conséquent, les réactions ont été effectuées dans une zone fermée, pour recycler les réactifs non utilisés. La première étape de cette voie est la réaction d'une aniline avec l' orthoformiate de triéthyle . Dans l'usine de fabrication nommée, la 2,4-xylidine a été utilisée comme aniline . La réaction donne un ester de formimidate intermédiaire. Dans l'étape suivante, de la méthylamine est ajoutée, qui se combine avec l'ester de formimidate pour donner la formamidine souhaitée. Au fur et à mesure que les formamidines se forment, l' éthanol est libéré de la réaction chimique et est recyclé. C'est probablement la méthode la plus appropriée pour la synthèse de l'amitraze, car cette deuxième étape donne la N′ -2,4-diméthyl- N -méthylformamidine. Les groupes -NH libres de ces molécules réagissent les uns avec les autres pour finalement donner de l'amitraze. Les dernières étapes du processus de fabrication comprennent la cristallisation à partir d'alcool isopropylique , la filtration et le séchage. Ces dernières étapes doivent être effectuées par du personnel averti, qui porte des vêtements de protection complets avec un appareil respiratoire à pression positive.
Voie 2 : Formamide substitué + aniline :
La première étape de cette voie de synthèse vers une N-arylformamidine comme l'amitraze est la réaction d'un formamide substitué , généralement un dialkylformamide, avec une aniline . Pour obtenir de l'amitraz, le N-méthyl formamide et le chlorhydrate de 2,4 diméthyl aniline peuvent être utilisés (figure 2). Cette réaction est catalysée par la présence d'halogénures d'acide, tels que POCl 3 , SOCl 2 , COCl 2 , ou un halogénure d'arylsulfonyle, comme le chlorure de p-toluène sulfonyle (figure 2). Cela donne un intermédiaire, qui réagit davantage en tant que catalysé par l'acide p-toluène en N, N'-[(méthylimino) diméthylidyne] di-2,4-xylidine (amitraz). Alternativement, l' aniline de la première étape peut être remplacée par un arylformamide. De plus, le remplacement du dialkylformamide par une N- alkylpyrrolidone peut être utilisé pour obtenir des produits du groupe clenpyrine à partir de cette réaction.
voie 3 : arylisocyanate + formamide :
Pour réaliser cette réaction, un mélange approprié d'arylisocyanate et de formamide est chauffé et marqué par le dégagement de CO 2 , pour donner la formamidine souhaitée.
Métabolisme
Étant donné que l'utilisation la plus courante de l'amitraz est comme pesticide , il est important de considérer qu'entre les animaux et les plantes, des voies différentes de biotransformation se produisent souvent . La plupart des espèces animales, y compris les humains, peuvent métaboliser rapidement l'amitraze pour former six métabolites au cours de la biotransformation , N -méthyl- N′ -(2,4-xylyl)formamide, Form-2'4'xylidine, 4-N-Méthyl-formidoyl) amino -acide méta-toluique, acide 4-formamido-méta-toluique, acide 4-acétamido-méta-toluique et acide 4-amino-méta-toluique.
Chez le rat , la voie métabolique (figure 3) a été étudiée après administration par voie orale de 14 amitraz C-marqué, qui a été trouvé pour être efficacement métabolisé, dégradées et excrétées à quatre des métabolites dans l' urine et six dans les matières fécales. La voie ou le taux métabolique ne différaient pas entre les sexes.
Hornish et Nappier (1983) ont détecté que la voie métabolique après administration cutanée suit la même voie de dégradation qu'après absorption orale, car le composé parent, la N-méthyl-N'-(2,4-xylyl)formamidine et la forme-2' Le ,4'-xylidide a également été trouvé dans l'urine et le sang après administration cutanée. Chez l'homme, N -méthyl- N -(2,4-xylyl)formamidine, form-2',4'-xylidide, acide 4-amino- méta-toluique, 4-acétamido- méta-toluique et 4-formamido- méta -des acides toluiques ont également été reconnus dans l'urine, ce qui indique une voie métabolique identique ou similaire.
Comme illustré sur la figure 3, la première étape est une réaction d'hydrolyse en N-méthyl-N'-(2,4-xylyl)-formamidine, qui peut déjà être excrétée dans l'urine mais qui est toujours pharmacologiquement active. Selon la dose, la quantité de ce métabolite dans les urines peut varier de 4 % à faible dose à 23 % à 38 % à forte dose (par exemple chez le rat : 1 à 100 mg par kg de poids corporel). Comme il n'est pas excrété, il peut également être oxydé en acide 4-N-méthyl-formidoyl)amino-méta-toluique, qui peut être encore oxydé en acide 4-formamido-méta-toluique. La forme-2,4-xylidine est formée directement par hydrolyse à partir de l'amitraze ou provient de la N-méthyl-N'-(2,4-xylyl)formamidine. Au cours de cette étape précoce de la biotransformation, la N-méthyl-N'-(2,4-xylyl)formamidine et la Forme-2,4-xylidine peuvent déjà former des conjugués. Mais la principale voie suivie après la formation de la forme-2,4-xylidine est l'oxydation en acide 4-formamido-méta-toluique, qui est ensuite métabolisé en son conjugué acétyle, l'acide 4-acétamido-méta-toluique ou 4-amino - acide méta-toluique. L'acide 4-formamido-méta-toluique et l'acide 4-acétamido-méta-toluique représentent 32 % des métabolites trouvés dans l'urine et sont détectés à n'importe quelle dose administrée. Par conséquent, ils sont considérés comme deux des principaux métabolites de la voie de l'amitraze. La forme-2',4'-xylidide et l'acide 4-amino-méta-toluique ne représentent que 2 % de l'excrétion totale. Chez les insectes, différents métabolites sont formés. La N-méthyl-N'-(2,4-xylyl)formamidine, la forme-2,4-xylidine et l'acide 4-amino-méta-toluique sont présents, mais en plus plusieurs métabolites non identifiés ont également été détectés.
Chez les plantes, la biotransformation de l'amitraze se déroule très rapidement. Les principaux métabolites détectés sont le N-(2,4-diméthylphényl)-N'-méthylformamidine (BST 27 271) et le 2,4-diméthylformanilide (BST 27 919).
La N-(2,4-diméthylphényl)-N'-méthylformamidine (BST 27 271), le 2,4-diméthylformanilide (BST 27 919) et la N,N'-bis-diméthylphénylformamidine (BTS 28 037) résultent de l' hydrolyse de l'amitraze. Ainsi, la N-(2,4-diméthylphényl)-N'-méthylformamidine (BST 27 271) est présente en quantités plus élevées que le 2,4-diméthylformanilide (BST 27 919). La N-(2,4-diméthylphényl)-N'-méthylformamidine (BST 27 271) peut être métabolisée en 2,4-diméthylformanilide (BST 27 919) ou en 2,4-diméthylaniline (BTS 24 868).
La N,N'-bis-diméthylphénylformamidine (BTS 28 037) peut être transformée en 2,4-diméthylformanilide (BST 27 919) ou réagir directement en 2,4-diméthylaniline (BTS 24 868), mais les mécanismes exacts de ces biotransformations sont pas encore connu. Cependant, moins de 1 % de la 2,4-diméthylaniline (BTS 24 868) et de la N,N'-bis-diméthylphénylformamidine (BTS 28 037) a été comptabilisée, ce qui en fait des métabolites mineurs par rapport à la N-(2,4-diméthylphényle )-N'-méthylformamidine (BST 27 271) et 2,4-diméthylformanilide (BST 27 919). La figure 4 montre la voie métabolique suggérée de l'amitraze chez les plantes.
Cinétique
Les réactions d' hydrolyse de l'amitraze dépendent fortement du pH environnemental. Même si l'amitraze subit des réactions d' hydrolyse à n'importe quel pH, des études de spectrophotométrie , HPLC et GC-MS ont révélé que des différences en fonction du pH se produisent, affectant à la fois le type de produits de réaction et la vitesse de réaction. Dans des conditions basiques (pH>6), l'amitraze est métabolisé en 2,4-diméthylphénylformamide. Suivie d'une hydrolyse en 2,4-diméthylaniline, qui bénéficie également d'un pH basique. À pH très acide (pH<3), la 2,4-diméthylaniline a été observée comme principal produit de dégradation. Dans des conditions moins acides (pH 3-6), on trouve principalement de la N-(2,4-diméthylphényl)-N′-méthylformamidine et déjà des quantités de 2,4-diméthylphénylformamide.
Mécanisme d'action
L'amitraze est utilisé comme pesticide . Par conséquent, l'exposition à l'amitraze chez les humains se produit principalement par inhalation ou par contact cutané avec le composé au cours de son utilisation ou de sa production. Les effets toxiques pour l'homme suite à l'absorption d'amitraz comprennent une perte de conscience, des vomissements, une insuffisance respiratoire, un myosis , une hypothermie , une bradycardie , une hyperglycémie et une dépression du système nerveux central .
L'activité pharmacologique de l'amitraze comprend différents mécanismes d'action conduisant à des effets toxiques chez l'homme ainsi que chez l'animal. Bon nombre de ces effets et la plupart des effets sur les humains sont causés par son activité agoniste alpha-adrénergique . De plus, l'amitraze inhibe la synthèse des prostaglandines , interagit avec les récepteurs octopamine du système nerveux central et inhibe les monoamine oxydases .
Des études chez l'animal ont révélé que les dommages dus à l'empoisonnement à l'amitraze peuvent être récupérés même après une exposition à une dose potentiellement mortelle . Cela pourrait signifier que les effets de l'amitraze sont réversibles ou au moins récupérables. Lorsqu'un empoisonnement à l'amitraze est mortel, la mort résulte d'une dépression respiratoire.
Activité agoniste alpha-adrénergique
L'amitraze est un agoniste central des récepteurs alpha-adrénergiques. Cela signifie qu'il stimule sélectivement les récepteurs alpha-adrénergiques , qui sont des récepteurs métabotropes couplés aux protéines G, qui sont généralement ciblés par les catécholamines . La stimulation de ces récepteurs est en grande partie à l'origine des effets neurotoxiques et préconvulsivants de l'amitraz. Le xylène présent dans les formulations d'amitraz induit en outre une dépression du système nerveux central . Les récepteurs adrénergiques peuvent être divisés en deux sous-classes, les récepteurs alpha1- et alpha2-adrénergiques. Pour déterminer si l'amitraze interagit avec la sous-classe 1 ou la sous-classe 2, des injections sous-cutanées d'amitraze (0,3 à 3,0 mg/kg) ont été administrées à des souris. Par conséquent, un retard dépendant de la dose du transit gastro - intestinal chez les souris conscientes se produit. Cet effet pourrait être antagonisé par des agents bloquants alpha2-adrénergiques, mais l'administration d'autres antagonistes n'a pas réduit l'effet dépresseur sur le transit gastro - intestinal . Il est donc suggéré que le retard du transit gastro - intestinal induit par l'amitraze est médié par les récepteurs alpha2-adrénergiques postjonctionnels et ne semble pas impliquer l'activation des récepteurs β-adrénergiques, dopaminergiques , sérotoninergiques , histaminergiques , cholinergiques , GABAergiques ou opioïdes . Outre les effets neurotoxiques, d'autres effets cliniques observés dans l'empoisonnement à l'amitraze sont liés à l'activité agoniste alpha2-adrénergique. Les récepteurs adrénergiques sont présents dans de nombreuses cellules différentes. L'activation de ces récepteurs par un agoniste comme l'amitraze induit généralement une réponse sympathique . Cela entraîne une augmentation de la fréquence cardiaque, une dilatation des pupilles, une élévation de la pression artérielle et une concentration de l'apport sanguin et énergétique sur les muscles squelettiques.
Interaction avec le récepteur de l'octopamine
On pense que le mode d'action de l'amitraze implique l'interaction avec le neuromodulateur octopamine . Cette interaction est probablement la raison de l'augmentation de l'activité nerveuse des tiques en réponse à l'amitraze. L'activation habituelle des récepteurs peut entraîner des changements dans la concentration de seconds messagers intracellulaires tels que les nucléotides cycliques AMP cyclique (AMPc) et GMP cyclique , l' inositol-1,4,5-triphosphate et le Ca 2+ . Influencer ce système de transduction de signal peut conduire à divers événements selon le type cellulaire. Depuis qu'il a été découvert que le gène codant pour le récepteur de l' octopamine est exprimé à des taux très élevés dans les somata du cerveau des abeilles, il est suggéré qu'il est impliqué dans le traitement des entrées sensorielles, des sorties motrices des antennes et des fonctions cérébrales d'ordre supérieur. L' interaction récepteur d' amitraz- octopamine restreint ces fonctions normales du récepteur d' octopamine . Par conséquent, il est efficace comme insecticide-pesticide. Pourtant, la résistance contre l'amitraze peut se produire. Une mutation peut conduire à une version fonctionnelle du récepteur d' octopamine mais avec un côté cible de pesticide modifié. C'est probablement le cas d'une souche de tique brésilienne et mexicaine très résistante, qui présente deux substitutions nucléotidiques sur le gène codant pour le récepteur de l' octopamine par rapport aux souches australiennes. Une meilleure compréhension de ces mécanismes de résistance aiderait à développer des outils de diagnostic plus rapides et plus précis pour détecter la résistance et orienter le développement d' acaricides alternatifs .
Inhibition des monoamine oxydases
In vitro, un effet inhibiteur de la monoamine oxydase de l'amitraze a été trouvé. Les monoamine oxydases catalysent la désamination oxydative des monoamines et forment ainsi des flavoprotéines et inactivent les neurotransmetteurs . Cependant, in vivo, il a été observé que ce n'est qu'à des doses élevées d'amitraz ou de son principal métabolite, la N -2,4-diméthylphényl- N -méthyl-formamide monoamine oxydase, qu'une inhibition se produit. Chez le chien, il a été observé qu'après l'administration d'une telle dose, une augmentation de la glycémie plasmatique et une suppression de l' insuline se produisent.
Inhibition de la synthèse des prostaglandines
Comme d'autres formamidines, l'amitraze inhibe la synthèse de la prostaglandine E2 à partir de l'acide arachidonique par les microsomes des vésicules séminales bovines. À une dose de 5 à 80 mg/kg de poids corporel, administrée par voie intrapéritonéale à des rats, l'amitraze réduit la fièvre induite par les levures et antagonise le gonflement de la patte arrière induit par la carraghénine. Certains des effets physiologiques de l'amitraze remontent probablement à cette activité semblable à l'aspirine et se produisent en raison de l'inhibition de la synthèse des prostaglandines.
Voir également
Les références
Liens externes
- L'amitraze dans la base de données sur les propriétés des pesticides (PPDB)




