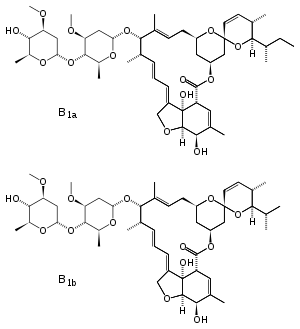
Avermectine - Avermectin
Les avermectines sont une série de médicaments et de pesticides utilisés pour traiter les vers parasites et les insectes nuisibles . Il s'agit d'un groupe de dérivés lactones macrocycliques à 16 chaînons dotés de puissantes propriétés anthelminthiques et insecticides . Ces composés naturels sont générés sous forme de produits de fermentation par Streptomyces avermitilis , un actinomycète du sol . Huit avermectines différentes ont été isolées dans quatre paires de composés homologues, avec un composant majeur (composant a) et mineur (composant b) généralement dans des rapports de 80:20 à 90:10. D'autres anthelminthiques dérivés des avermectines comprennent l' ivermectine , la sélamectine , la doramectine , l' éprinomectine et l' abamectine .
La moitié du prix Nobel de physiologie ou médecine 2015 a été décernée à William C. Campbell et Satoshi Ōmura pour la découverte de l'avermectine, « dont les dérivés ont radicalement réduit l'incidence de la cécité des rivières et de la filariose lymphatique , tout en montrant une efficacité contre un nombre croissant d'autres maladies parasitaires."
Histoire
En 1978, un actinomycète a été isolé à l' Institut Kitasato à partir d'un échantillon de sol collecté à Kawana, Ito City , Shizuoka Prefecture, Japan. Plus tard dans l'année, l'actinomycète isolé a été envoyé aux laboratoires de recherche Merck Sharp et Dohme pour être testé. Divers bouillons soigneusement contrôlés ont été fermentés en utilisant l'actinomycète isolé. Les premiers tests ont indiqué que certains des bouillons fermentés entiers étaient actifs contre Nematospiroides dubius chez la souris sur au moins une plage de huit fois sans toxicité notable. Par la suite, l'activité anthelminthique a été isolée et identifiée comme une famille de composés étroitement apparentés. Les composés ont finalement été caractérisés et les nouvelles espèces qui les ont produits ont été décrites par une équipe de Merck en 1978 et nommées Streptomyces avermitilis (avec l'adjectif probablement destiné à signifier qu'il tue les vers).
En 2002, Yoko Takahashi et d'autres du Kitasato Institute for Life Sciences de l'Université de Kitasato et du Kitasato Institute ont proposé que Streptomyces avermitilis soit renommé Streptomyces avermectinius .
Dosage
Une thérapie couramment utilisée ces derniers temps a été basée sur l'administration orale, parentérale , topique ou localisée (comme dans les "gouttes" vétérinaires anti-puces) d'avermectines. Ils montrent une activité contre un large éventail de nématodes et d' arthropodes parasites des animaux domestiques à des doses de 300 g/kg ou moins (200 μg/kg d'ivermectine semblant être la norme interspécifique commune, des humains aux chevaux aux animaux domestiques, sauf indication contraire ). Contrairement aux antibiotiques macrolides ou polyènes , ils manquent d'activités antibactériennes ou antifongiques significatives.
Mécanisme d'action
Les avermectines bloquent la transmission de l'activité électrique dans les cellules nerveuses et musculaires des invertébrés principalement en améliorant les effets du glutamate au niveau du canal chlorure glutamate-dépendant qui est spécifique aux invertébrés protostomiens , avec des effets mineurs sur les récepteurs de l'acide gamma-aminobutyrique . Cela provoque un afflux d'ions chlorure dans les cellules, entraînant une hyperpolarisation et une paralysie subséquente des systèmes neuromusculaires des invertébrés; des doses comparables ne sont pas toxiques pour les mammifères car ils ne possèdent pas de canaux chlorure glutamate-dépendants spécifiques du protostome .
Toxicité et effets secondaires
Une résistance aux avermectines a été rapportée, ce qui suggère une utilisation modérée. La résistance chez Caenorhabditis elegans a été observée par la voie la plus évidente - la variation du canal chlorure glutamate-dépendant . Les recherches sur l' ivermectine , la pipérazine et le dichlorvos en combinaison montrent également un potentiel de toxicité. Il a été rapporté que l'avermectine bloque la sécrétion induite par le LPS du facteur de nécrose tumorale , de l' oxyde nitrique , de la prostaglandine E2 et l'augmentation de la concentration intracellulaire de Ca 2+ . Les effets indésirables sont généralement transitoires ; les effets graves sont rares et ne surviennent probablement qu'en cas de surdosage important, mais comprennent le coma , l' hypotension et l' insuffisance respiratoire , pouvant entraîner la mort. Il n'existe pas de traitement spécifique, mais la prise en charge symptomatique conduit généralement à un pronostic favorable.
Biosynthèse de l'avermectine
Le groupe de gènes pour la biosynthèse de l'avermectine de S. avermitilis a été séquencé. Le groupe de gènes de biosynthèse de l'avermectine code pour des enzymes responsables de quatre étapes de la production d'avermectine : 1) la production de l' aglycone de l'avermectine par les polykétides synthases , 2) la modification de l'aglycone, 3) la synthèse des sucres modifiés et 4) la glycosylation de l'aglycone de l'avermectine modifié. Ce groupe de gènes peut produire huit avermectines qui présentent des différences structurelles mineures.
L'aglycone initial de l'avermectine est synthétisé par l' activité polykétide synthase de quatre protéines (AVES 1, AVES 2, AVES 3 et AVES 4). L'activité de ce complexe enzymatique est similaire à celle des polykétide synthases de type I. Le 2-méthylbutyrl CoA ou l'isobutyrl CoA peuvent être utilisés comme unités de départ et sont prolongés par sept unités acétate et cinq unités propionate pour produire respectivement la série "a" ou la série "b" de l'avermectine. L'aglycone initial est ensuite libéré du domaine thioestérase d'AVES 4 par formation d'un ester cyclique intramoléculaire .
L'aglycone initial de l'avermectine est encore modifié par d'autres enzymes du groupe de gènes biosynthétiques de l'avermectine. L'AveE a une activité monooxygénase du cytochrome P450 et facilite la formation du cycle furane entre C6 et C8. AveF a une activité de cétoréductase NAD(P)H-dépendante qui réduit le groupe céto C5 en un hydroxyle. AveC influence l'activité de la déshydratase dans le module deux (affectant C22-C23), bien que le mécanisme par lequel il le fait ne soit pas clair. AveD a une activité C5 O-méthyltransférase dépendante de SAM. Que l'AveC ou l'AveD agisse sur l'aglycone détermine si l'aglycone d'avermectine résultant produira des séries d' avermectine « A » ou « B » et des séries 1 ou 2 , respectivement.
Neuf cadres de lecture ouverts (orf1 et aveBI-BVIII) sont en aval de aveA4, qui sont connus pour être impliqués dans la glycosylation et la synthèse des sucres. AveBII-BVIII sont responsables de la synthèse de dTDP-L-oléandrose et AveBI est responsable de la glycosylation de l'aglycone de l'avermectine avec le dTDP-sucre. La séquence d'orf1 suggère que son produit aura une activité réductase, mais cette fonctionnalité ne semble pas nécessaire à la synthèse de l'avermectine.
Autres utilisations
L'abamectine est l'ingrédient actif de certains pièges à fourmis commerciaux.
Voir également
- Les milbémycines sont un groupe chimiquement étroitement apparenté de parasiticides.
- La glycorandomisation avermectine/ivermectine a conduit à une gamme de nouveaux analogues glycosylés différentiellement.