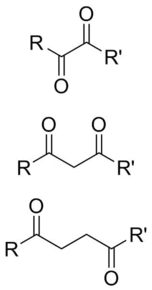
Dicarbonyle - Dicarbonyl
Un dicarbonyle est une molécule contenant deux groupes carbonyle (C = O) . Bien que ce terme puisse faire référence à tout composé organique contenant deux groupes carbonyle, il est utilisé plus spécifiquement pour décrire des molécules dans lesquelles les deux carbonyles sont suffisamment proches pour que leur réactivité soit modifiée, comme 1,2-, 1,3- et 1,4-dicarbonyles. Leurs propriétés diffèrent souvent de celles des monocarbonyles et sont donc généralement considérés comme des groupes fonctionnels à part entière. Ces composés peuvent avoir des substituants symétriques ou asymétriques sur chaque carbonyle, et peuvent également être fonctionnellement symétriques (dialdéhydes, dicétones, diesters, etc. ) ou asymétriques (céto-esters, céto-acides, etc. ).
1,2-Dicarbonyles
1,2-dialdéhyde
Le seul 1,2-dialdéhyde est le glyoxal , (CHO) 2 . Comme de nombreux alkyldialdéhydes, le glyoxal est rencontré presque exclusivement sous forme d'hydrate et d'oligomères de celui-ci. Ces dérivés se comportent souvent de manière équivalente aux aldéhydes car l'hydratation est réversible. Le glyoxal se condense facilement avec les amines . Via de telles réactions, c'est un précurseur de nombreux hétérocycles , par exemple les imidazoles .

1,2-Dicétones
La principale dicétone est le diacétyle , également connu sous le nom de 2,3-butanedione, CH 3 C(O)C(O)CH 3 . Les 1,2-dicétones sont souvent générées par oxydation (déshydrogénation) des diols :
- RCH (OH) CH (OH) R → RC (O) C (O) R + 2 H 2
La 2,3-butanedione, la 2,3-pentanedione et la 2,3-hexanedione se trouvent en petites quantités dans divers aliments. Ils sont utilisés comme composants aromatiques dans les boissons sans alcool et dans les produits de boulangerie. Benzil , (PhCO) 2 , est le dérivé diphényle correspondant.
Une caractéristique distinctive des 1,2-dicétones est la longue liaison CC liant les groupes carbonyle. Cette distance de liaison est d'environ 1,54 Â, contre 1,45 Â pour la liaison correspondante dans le 1,3-butadiène . L'effet est attribué à la répulsion entre les charges positives partielles des atomes de carbone carbonyle.
Les 1,2-dicétones se condensent avec de nombreux nucléophiles bifonctionnels, tels que l' urée et la thiourée, pour donner des hétérocycles. La condensation avec des amines aromatiques donne la dicétimine ((RC = NAr) 2 ).
Dans les cas de la 1,2-cyclohexanedione et de la 1,2-cyclopentanedione , l' énol est environ 1-3 kcal/mol plus stable que la forme dicéto.
ortho-Quinone , C 4 H 4 (CO) 2 , est le parent d'une grande famille de 1,2-dicétones.
1,2-diesters et diacides
L'acide oxalique et ses esters définissent cette famille de composés. Le diacide est produit industriellement par oxydation des sucres résiduaires. Il se produit naturellement (comme base conjuguée), notamment chez les membres de l'espèce végétale Oxalis . La condensation des diesters avec les diamines donne des diamides cycliques.
Acides α-céto et formylcarboxyliques

Les α-céto-acides et les esters sont bien connus. L'acide pyruvique (CH 3 C(O)CO 2 H) est le parent -cétoacide. Sa base conjuguée, le pyruvate (CH 3 C (O) CO 2 - ), est un composant du cycle de l'acide citrique et produit du métabolisme du glucose ( glycolyse ). L'aldéhyde-acide correspondant est l'acide glyoxalique (HC(O)CO 2 H).
1,3-dicarbonyles
1,3-dialdéhydes
Le 1,3-dialdéhyde parent est le malondialdéhyde (CH 2 (CHO) 2 ). Comme la plupart des dialdéhydes, il est rarement rencontré en tant que tel. Au lieu de cela, il est traité presque exclusivement sous forme d'hydrate, d'acétal de méthyle et d'oligomères de celui-ci. Ces dérivés se comportent souvent comme le parent. De nombreux dérivés substitués en 2 sont connus. Ils sont souvent préparés par alkylation de l' énolate de malondialdéhyde.
1,3-dicétones
Un membre important est l' acétylacétone , CH 3 C (O) CH 2 C (O) CH 3 . Dimedone est une 1,3-dicétone cyclique. L'acétylacétone est préparée industriellement par réarrangement thermique de l'acétate d'isopropényle. Une autre 1,3-dicétone cyclique est la 2,2,4,4-tétraméthylcyclobutanedione , qui est un précurseur d'un diol utile .
- CH 2 (CH 3 )COC(O)Me → MeC(O)CH 2 C(O)Me
1,3-dicétones qui peuvent tautomériser à un énol qui est conjugué à l'autre carbonyle existent habituellement principalement sous la forme énol, et en particulier lorsque peuvent être encore stabilisés produit par un cycle à six chaînons contenant une liaison hydrogène. Par exemple, le pourcentage d'énol dans l' acétylacétone , la trifluoroacétyacétone et l' hexafluoroacétylacétone sont de 85, 97 et 100%, respectivement (pur, 33 ° C).
Comme d'autres dicétones, les 1,3-dicétones sont des précurseurs polyvalents d'hétérocycles. L'hydrazine , par exemple, se condense pour donner des pyrazoles .
La base conjuguée dérivée de 1,3-cétones peut servir de ligand pour former des complexes de coordination d'acétylacétonate de métal . Dans la réaction de DeMayo, les 1,3-dicétones réagissent avec les alcènes dans une réaction photochimique péricyclique pour former des 1,5-dicétones (substituées).
Classiquement, les 1,3-dicétones sont préparées par condensation de Claisen d'une cétone avec un ester.
1,3-Diesters et diacides
L'acide malonique et ses esters sont les membres parents de cette classe de dicarbonyles. Sont également courants les dérivés 2-substitués de formule RCH(CO 2 R) 2 , qui surviennent par C-alkylation de la base conjuguée (l'énolate) NaCH(CO 2 R) 2 .
β-céto-esters
Les ß-céto-esters apparaissent facilement par condensation d'une paire d'esters. Un exemple bien connu est l'acétoacétate d'éthyle (bien qu'il soit préparé par éthanolyse du cétène ).
1,4-dicarbonyles
1,4-dialdéhydes
Le succinaldéhyde (CH 2 CHO) 2 est le 1,4-dialdéhyde le plus simple et le parent.
1,4-dicétones

Les dicétones avec deux groupes méthylène séparant les groupes carbonyle, également appelés γ-dicétones, coexistent généralement avec leurs tautomères énol . Le membre prééminent est l' acétonylacétone . Les 1,4-dicétones sont des précurseurs utiles des hétérocycles via la synthèse de Paal-Knorr , qui donne des pyrroles :
Cette réactivité est à la base de la neurotoxicité des γ-dicétones. Les 1,4-dicétones sont également des précurseurs des furanes et des thiophènes . La condensation de 1,4-dicétones (et de substrats apparentés) avec des hydrazines donne des dihydropyridazines, qui peuvent être converties en pyridazines .
la para-quinone , C 4 H 4 (CO) 2 , est le parent d'une grande famille de 1,4-dicétones.
1,4-diesters et diacides
L'acide succinique et ses esters sont les membres parents de cette famille de 1,4-dicarbonyles. L'acide succinique est remarquable en tant que composant dans le cycle de l'acide citrique . Il forme un anhydride d'acide cyclique, l'anhydride succinique . Les membres insaturés comprennent les acides et esters maléique et fumarique .
1,5-Dicarbonyles
1,5-dialdéhydes
Le glutaraldéhyde (CH 2 ) 3 (CHO) 2 est le 1,5-dialdéhyde le plus simple et le plus parent. Il s'hydrate facilement. L'analogue aromatique est l' isophtalaldéhyde .
1,5-dicétones
Ces dicétones ont trois groupes méthylène séparant les groupes carbonyle.
1,5-diesters et diacides
L'acide glutarique (CH 2 ) 3 (CO 2 H) 2 est le 1,5-diacide parent.
Hydratation et cyclisation

Les petits aldéhydes ont tendance à s'hydrater. L'hydratation est prédominante pour les dialdéhydes. Le glyoxal forme une série d'hydrates cycliques. Le succinaldéhyde s'hydrate facilement pour donner du 2,5-dihydroxytétrahydrofurane. Le phtalaldéhyde aromatique se forme également hydraté.
Des équilibres d'hydratation et de cyclisation similaires s'appliquent au dialdéhyde maléique, au glutaraldéhyde et à l'adipaldéhyde.
Sécurité
Un certain nombre de composés dicarbonylés sont bioactifs. Le diacétyle est connu pour causer la bronchiolite oblitérante de la maladie pulmonaire chez les personnes qui y sont exposées dans un cadre professionnel. Les dialdéhydes, par exemple le glutaraldéhyde et le malonaldéhyde, sont des fixateurs ou des stérilisateurs.