Irinotécan - Irinotecan
 | |
 | |
| Donnée clinique | |
|---|---|
| Appellations commerciales | Camptosar, Campto, Onivyde, autres |
| AHFS / Drugs.com | Monographie |
| MedlinePlus | a608043 |
| Données de licence | |
Catégorie grossesse |
|
| Voies administratives |
Intraveineux |
| code ATC | |
| Statut légal | |
| Statut légal | |
| Données pharmacocinétiques | |
| Biodisponibilité | N / A |
| Métabolisme | foie glucuronidation |
| Demi-vie d' élimination | 6 à 12 heures |
| Excrétion | Biliaire et rein |
| Identifiants | |
| |
| Numero CAS | |
| CID PubChem | |
| IUPHAR/BPS | |
| Banque de médicaments | |
| ChemSpider | |
| UNII | |
| KEGG | |
| ChEBI | |
| ChEMBL | |
| Tableau de bord CompTox ( EPA ) | |
| Carte d'information de l'ECHA |
100.219.260 |
| Données chimiques et physiques | |
| Formule | C 33 H 38 N 4 O 6 |
| Masse molaire | 586,689 g·mol -1 |
| Modèle 3D ( JSmol ) | |
| |
| |
|
| |
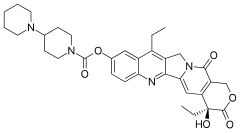
L'irinotécan , vendu entre autres sous la marque Camptosar , est un médicament utilisé pour traiter le cancer du côlon et le cancer du poumon à petites cellules . Pour le cancer du côlon, il est utilisé seul ou avec du fluorouracile . Pour le cancer du poumon à petites cellules, il est utilisé avec le cisplatine . Il est administré par voie intraveineuse .
Les effets secondaires courants comprennent la diarrhée , les vomissements , la suppression de la moelle osseuse , la perte de cheveux, l'essoufflement et la fièvre. D'autres effets secondaires graves incluent des caillots sanguins , une inflammation du côlon et des réactions allergiques . Ceux qui ont deux copies de la variante du gène UGT1A1*28 sont plus à risque d'effets secondaires. L'utilisation pendant la grossesse peut nuire au bébé. L'irinotécan est un inhibiteur de la topoisomérase - il bloque l' enzyme topoisomérase 1 , entraînant des dommages à l' ADN et la mort cellulaire .
L'irinotécan a été approuvé à des fins médicales aux États-Unis en 1996. Il figure sur la liste des médicaments essentiels de l'Organisation mondiale de la santé . Il est fabriqué à partir du composé naturel camptothécine que l'on trouve dans l'arbre ornemental chinois Camptotheca acuminata .
Utilisations médicales
Son utilisation principale est dans le cancer du côlon , en particulier, en association avec d'autres agents chimiothérapeutiques. Cela comprend le régime FOLFIRI , qui consiste en une perfusion de 5-fluorouracile , de leucovorine et d' irinotécan . Le schéma thérapeutique XELIRI comprend la capécitabine et l'irinotécan.
Il peut également être utilisé avec le fluorouracile et l'acide folinique pour le cancer du pancréas après l'échec du traitement initial.
Effets secondaires
Les effets indésirables les plus importants de l'irinotécan sont la diarrhée, les nausées et les vomissements, la neutropénie et la fièvre, les infections du sang ou des poumons (septicémie, pneumonie), le choc, la déshydratation, l'insuffisance rénale et la thrombocytopénie (faibles taux de plaquettes sanguines).
La diarrhée
La diarrhée associée à l'irinotécan est sévère et cliniquement significative, conduisant parfois à une déshydratation sévère nécessitant une hospitalisation ou une admission en unité de soins intensifs. Cet effet secondaire est géré par l'utilisation agressive d'antidiarrhéiques tels que le lopéramide ou l' atropine dès les premières selles molles.
Immunosuppression
L'irinotécan a un impact négatif sur le système immunitaire. Cela se traduit par une baisse – parfois dramatique – du nombre de globules blancs dans le sang, en particulier les neutrophiles . Le patient peut présenter une neutropénie (une diminution cliniquement significative des neutrophiles dans le sang).
Mécanisme d'action
La camptothécine, l'une des quatre principales classifications structurelles des composés anticancéreux d'origine végétale, est un alcaloïde cytotoxique qui se compose d'une structure cyclique pentacyclique contenant un fragment quinoléine pyrrole (3, 4 ), une forme lactone à configuration S et une forme carboxylate. L'irinotécan est activé par hydrolyse en SN-38 , un inhibiteur de la topoisomérase I. Celui-ci est ensuite inactivé par glucuronidation par l'uridine diphosphate glucuronosyltransférase 1A1 ( UGT1A1 ). L'inhibition de la topoisomérase I par le métabolite actif SN-38 conduit finalement à l'inhibition à la fois de la réplication et de la transcription de l'ADN.
L'action moléculaire de l'irinotécan se produit en piégeant un sous-ensemble de complexes de clivage de la topoisomérase -1-ADN, ceux avec une guanine +1 dans la séquence d'ADN. Une molécule d'irinotécan s'empile contre les paires de bases flanquant le site de clivage induit par la topoisomérase et empoisonne (inactive) l' enzyme topoisomérase 1.
Parcours interactif
Cliquez sur les gènes, les protéines et les métabolites ci-dessous pour accéder aux articles respectifs.
Pharmacocinétique
Administration
L'irinotécan peut être administré par perfusions intraveineuses de 30 ou 90 minutes de 125 mg/m 2 par semaine pendant quatre semaines sur six ou de 350 mg/m 2 toutes les trois semaines.
Distribution
L'irinotécan est un composé hydrophile avec un grand volume de distribution (400 L/m 2 ). Au pH physiologique, l'irinotécan et son métabolite actif éthyl-10-hydroxy-camptothécine (SN-38) sont présents sous deux isoformes à l'équilibre pH-dépendantes; le cycle lactone actif anti-tumeur qui s'hydrolyse en l'isoforme carboxylate.
Dans le plasma, la majorité de l'irinotécan et du SN-38 sont liés à l'albumine, ce qui stabilise leurs formes lactones. Dans le sang, l'irinotécan et le SN-38 sont liés aux plaquettes et aux globules rouges.
L'irinotécan a une pharmacocinétique linéaire. Les modèles pharmacocinétiques de population supposaient un modèle à trois compartiments pour l'irinotécan et un modèle à deux compartiments pour le SN-38.
Le SN-38 a une demi-vie de distribution courte (environ 8 min). Il a atteint son pic de concentration plasmatique dans les 2 heures suivant la perfusion. Le SN-38 présente également un deuxième pic de concentration plasmatique en raison de sa recirculation entérohépatique et de sa libération par les érythrocytes.
Métabolisme
Activation par les carboxylestérases et les butyrylcholinestéras
Environ 2 à 5 % du promédicament irinotécan est hydrolysé en son métabolite actif SN-38 dans le foie par deux enzymes de conversion de la carboxylestérase (CES1 et CES2) et dans le plasma par la butyrylcholinestérase (hBChE). CES2 a une affinité 12,5 fois plus élevée pour l'irinotécan que CES1. Alors que la butyrylcholinestérase a une activité 6 fois plus élevée pour l'irinotécan que la CES. Après conversion, le SN-38 est activement transporté vers le foie par le transporteur 1B1 du polypeptide de transport d'anions organiques (OATP).
Inactivation par les uridine diphosphate glucuronosyltransférases
Le SN-38 est inactivé par glucuronidation en SN-38G (conjugué β-glucuronide) par plusieurs enzymes uridine diphosphate glucuronosyltransférase (UGT) dans le foie (UGT1A1, UGT1A9) et extra-hépatique (UGT1A1, UGT1A7, UGT1A10) et excrété dans le foie . Plusieurs polymorphismes de l'UGT affectent la pharmacocinétique de l'irinotécan, par exemple, la diminution de l'activité de l'UGT1, peut entraîner une toxicité sévère. De plus, l'UGT1A1 conjugue la bilirubine et la glucuronidation de la bilirubine est un autre facteur de risque d'augmentation de la toxicité
Déconjugaison par les -glucuronidases
Les bactéries intestinales ont produit des -glucuronidases qui dé-conjuguent le SN-38G en SN-38, entraînant une recirculation entéro-hépatique du SN-38.
Métabolisme par les enzymes du cytochrome P450
L'irinotécan est métabolisé par les enzymes intrahépatiques du cytochrome P450, CYP3A4 et CYP3A5 en métabolites inactifs APC (7-éthyl-10-[4-N-(5-aminopentanoïque acide)-1-pipéridino] carbonyloxycamptothécine) et NPC (7-éthyl-10- [4-amino-1-pipéridino] carbonyloxycamptothécine). NPC peut encore être converti par CES1 et CES2 dans le foie en SN-38. L'induction ou l'inhibition des enzymes CYP3A par le tabagisme, certaines herbes et certains médicaments peuvent entraîner des interactions avec l'irinotécan.
Transport vers la bile
L'irinotécan est transporté dans la bile par les protéines de transport de la cassette de liaison à l'ATP (ABC) : ABCB1, ABCC1, ABCC2 et ABCG2.
Élimination
La clairance de l'irinotécan est principalement biliaire (66 %) et estimée à 12-21 L/h/m 2 . Tous les métabolites, à l'exception du SN-38G, sont principalement excrétés dans les fèces. Les demi-vies d'élimination de l'irinotécan ont été rapportées entre 5 et 18 h. Les demi-vies du SN-38 ont été signalées entre 6 et 32 h.
Il existe une forte variabilité interindividuelle (30 %) des paramètres pharmacocinétiques de l'irinotécan qui peuvent être modifiés par plusieurs facteurs, notamment l'âge, le sexe, la dose, le moment de l'administration, la fonction hépatique, l'activité enzymatique ou les taux d'hématocrite.
Pharmacogénomique
L'irinotécan est converti par une enzyme en son métabolite actif SN-38, qui est à son tour inactivé par l'enzyme UGT1A1 par glucuronidation.
*28 patients variants
Les personnes atteintes de variantes de l'UGT1A1 appelées TA 7 , également connues sous le nom de "variante * 28", expriment moins d'enzymes UGT1A1 dans leur foie et souffrent souvent du syndrome de Gilbert . Pendant la chimiothérapie, ils reçoivent effectivement une dose plus importante que prévu parce que leur corps n'est pas en mesure d'éliminer l'irinotécan aussi rapidement que les autres. Dans les études, cela correspond à des incidences plus élevées de neutropénie sévère et de diarrhée.
En 2004, une étude clinique a été réalisée qui a à la fois validé prospectivement l'association du variant *28 avec une plus grande toxicité et la capacité des tests génétiques à prédire cette toxicité avant l'administration de la chimiothérapie.
En 2005, la FDA a apporté des modifications à l'étiquetage de l'irinotécan pour ajouter des recommandations pharmacogénomiques , de sorte que les receveurs d'irinotécan présentant un polymorphisme homozygote (les deux copies du gène) dans le gène UGT1A1, pour être précis, la variante *28, devraient être pris en considération pour doses médicamenteuses réduites. L'irinotécan est l'un des premiers agents chimiothérapeutiques largement utilisés qui est dosé en fonction du génotype du receveur.
Société et culture
Approbation
L'irinotécan a reçu une approbation accélérée de la Food and Drug Administration (FDA) des États-Unis en 1996 et une approbation complète en 1998.
Noms
Au cours du développement, il était connu sous le nom de CPT-11.
Formules
Une version encapsulée dans des liposomes de l'irinotécan vendue sous le nom d'Onivyde par Merrimack Pharmaceuticals a été approuvée par la FDA en octobre 2015 pour traiter le cancer du pancréas métastatique . Il a été approuvé pour un usage médical dans l'Union européenne en octobre 2016.
Voir également
- Etirinotecan pegol , un dérivé expérimental de l'irinotécan avec une demi-vie plus longue dans le corps humain
Les références
Lectures complémentaires
- Dean L (2015). "Thérapie Irinotécan et Génotype UGT1A1" . Dans Pratt VM, McLeod HL, Rubinstein WS et al. (éd.). Résumés de génétique médicale . Centre national d'information sur la biotechnologie (NCBI). PMID 28520360 . ID de la bibliothèque : NBK294473.
Liens externes
- "Irinotécan" . Portail d'information sur les médicaments . Bibliothèque nationale de médecine des États-Unis.
- "Chlorhydrate d'irinotécan" . Portail d'information sur les médicaments . Bibliothèque nationale de médecine des États-Unis.
- Irinotecan Pathway sur PharmGKB

