Noscapine - Noscapine
 | |
 | |
| Donnée clinique | |
|---|---|
| Autres noms | Narcotine |
| AHFS / Drugs.com | Noms internationaux des médicaments |
Catégorie grossesse |
|
| code ATC | |
| Statut légal | |
| Statut légal | |
| Données pharmacocinétiques | |
| Biodisponibilité | ~30% |
| Demi-vie d' élimination | 1,5 à 4h (moyenne 2,5) |
| Identifiants | |
| |
| Numero CAS | |
| CID PubChem | |
| ChemSpider | |
| UNII | |
| KEGG | |
| ChEBI | |
| ChEMBL | |
| Tableau de bord CompTox ( EPA ) | |
| Carte d'information de l'ECHA |
100.004.455 |
| Données chimiques et physiques | |
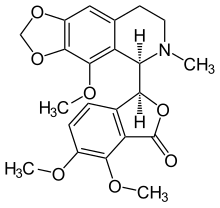
| Formule | C 22 H 23 N O 7 |
| Masse molaire | 413,421 g·mol -1 |
| Modèle 3D ( JSmol ) | |
| |
| |
|
| |
La noscapine (également connue sous le nom de Narcotine , Nectodon , Nospen , Anarcotine et (archaïque) Opiane ) est un alcaloïde benzylisoquinoléine , du sous-groupe structural des phtalideisoquinoléines, qui a été isolé à partir de nombreuses espèces de la famille des Papaveraceae (famille du pavot). Il manque d'effets hypnotiques, euphoriques ou analgésiques significatifs, ce qui lui confère un potentiel de dépendance très faible. Cet agent est principalement utilisé pour ses effets antitussifs (antitussifs).
Utilisations médicales
La noscapine est souvent utilisée comme médicament antitussif . Une directive néerlandaise de 2012 ne recommande cependant pas son utilisation pour la toux aiguë .
Effets secondaires
- La nausée
- Vomissement
- Perte de coordination
- Hallucinations (auditives et visuelles)
- Perte de libido
- Gonflement de la prostate
- Perte d'appétit
- Pupilles dilatées
- Rythme cardiaque augmenté
- Tremblements et spasmes musculaires
- Douleurs à la poitrine
- Vigilance accrue
- Perte de toute somnolence
- Perte de la vision stéréoscopique
Interactions
La noscapine peut augmenter les effets des substances sédatives telles que l'alcool et les hypnotiques .
Le médicament ne doit pas être pris avec des IMAO (inhibiteurs de la monoamine oxydase), car des effets inconnus et potentiellement mortels peuvent survenir.
La noscapine ne doit pas être prise en association avec la warfarine car les effets anticoagulants de la warfarine peuvent être augmentés.
Mécanisme d'action
Les effets antitussifs de la noscapine semblent être principalement médiés par son activité agoniste des récepteurs σ . La preuve de ce mécanisme est suggérée par des preuves expérimentales chez le rat. Un prétraitement par le rimcazole , un antagoniste -spécifique , provoque une réduction dose-dépendante de l'activité antitussive de la noscapine. La noscapine et ses dérivés synthétiques appelés noscapinoïdes sont connus pour interagir avec les microtubules et inhiber la prolifération des cellules cancéreuses
Analyse structurelle
L' anneau lactone est instable et s'ouvre dans les milieux basiques. La réaction inverse se présente en milieu acide. La liaison (C1-C3') reliant les deux atomes de carbone optiquement actifs est également instable. En solution aqueuse d'acide sulfurique et en chauffant il se dissocie en cotarnine (4-méthoxy-6-méthyl-5,6,7,8-tétrahydro-[1,3]dioxolo[4,5- g ]isoquinoléine) et en acide opique ( acide 6-formyl-2,3-diméthoxybenzoïque). Lorsque la noscapine est réduite avec du zinc / HCl , la liaison C1−C3′ se sature et la molécule se dissocie en hydrocotarnine (2-hydroxycotarnine) et méconine (6,7-diméthoxyisobenzofuran-1(3 H )-one).
Histoire
La noscapine a été isolée et caractérisée pour la première fois par sa décomposition chimique et ses propriétés en 1817 sous la dénomination de « Narcotine » par Pierre Robiquet , un chimiste français à Paris. Robiquet a mené pendant 20 ans entre 1815 et 1835 une série d'études sur l'amélioration des méthodes d'isolement de la morphine , et a également isolé en 1832 un autre composant très important de l'opium brut, qu'il a appelé codéine , actuellement un composé dérivé de l'opium largement utilisé. .
Société et culture
Utilisation récréative
Il existe des rapports anecdotiques sur l'utilisation récréative de médicaments en vente libre dans plusieurs pays, facilement disponibles dans les pharmacies locales sans ordonnance. Les effets, commençant environ 45 à 120 minutes après la consommation, sont similaires à ceux du dextrométhorphane et de l'intoxication alcoolique . Contrairement au dextrométhorphane, la noscapine n'est pas un antagoniste des récepteurs NMDA .
Noscapine dans l'héroïne
La noscapine peut survivre aux processus de fabrication de l' héroïne et peut être trouvée dans l'héroïne de rue. Ceci est utile pour les organismes d'application de la loi, car les quantités de contaminants peuvent identifier la source des drogues saisies. En 2005 à Liège , en Belgique , la concentration moyenne en noscapine était d'environ 8%.
La noscapine a également été utilisée pour identifier les toxicomanes qui prennent de l'héroïne de rue en même temps que la diamorphine prescrite . Étant donné que la diamorphine contenue dans l'héroïne de rue est la même que la diamorphine pharmaceutique, l'examen des contaminants est le seul moyen de vérifier si l'héroïne de rue a été consommée. D'autres contaminants utilisés dans les échantillons d' urine aux côtés de la noscapine comprennent la papavérine et l' acétylcodéine . La noscapine est métabolisée par l'organisme et est elle-même rarement retrouvée dans l'urine, étant plutôt présente sous forme de métabolites primaires, la cotarnine et la méconine . La détection est effectuée par chromatographie en phase gazeuse-spectrométrie de masse ou chromatographie liquide-spectrométrie de masse (LCMS), mais peut également utiliser une variété d'autres techniques analytiques.
Recherche
Essais cliniques
L'efficacité de la noscapine dans le traitement de certaines hémopathies malignes a été explorée en clinique. L' induction de polyploïdie par la noscapine a été observée in vitro dans des lymphocytes humains à des doses élevées (> 30 M); cependant, une exposition systémique de faible intensité, par exemple avec des médicaments contre la toux, ne semble pas présenter de risque génotoxique. Il est suggéré que le mécanisme d' induction de la polyploïdie par la noscapine implique soit des dommages à l' appareil du fuseau chromosomique , soit une fusion cellulaire.
Reconstitution de la biosynthèse de la noscapine
De nombreuses enzymes de la voie de biosynthèse de la noscapine ont été élucidées par la découverte d'un « cluster de type opéron » de 10 gènes nommé HN1. En 2016, la voie de biosynthèse de la noscapine a été reconstituée dans des cellules de levure, permettant au médicament d'être synthétisé sans avoir besoin de récolte et de purification à partir de matériel végétal. En 2018, toute la voie de la noscapine a été reconstituée et produite dans la levure à partir de molécules simples. De plus, l'expression des protéines a été optimisée chez la levure, permettant d'améliorer la production de noscapine de 18 000 fois. On espère que cette technologie pourra être utilisée pour produire des alcaloïdes pharmaceutiques tels que la noscapine qui sont actuellement exprimés à un rendement trop faible in plantae pour être produits en masse, leur permettant de devenir des médicaments thérapeutiques commercialisables.
Dérivés anticancéreux
La noscapine est elle-même un agent anti-mitiotique, par conséquent ses analogues ont un grand potentiel en tant que nouveaux médicaments anticancéreux. Des analogues ayant des effets cytotoxiques significatifs par le biais d'un fragment 1,3-benzodioxole modifié ont été développés. De même, des dérivés N-alkyl amine, 1,3-diynyl, 9-vinyl-phényl et 9-arylimino de la noscapine ont également été développés. Leur mécanisme d'action passe par l' inhibition de la tubuline .
Voir également
- Sirop pour la toux
- Codéine ; Pholcodine
- dextrométhorphane ; Dimemorfan
- Racemorphane ; Dextrorphane ; Lévorphanol
- Butamirate
- Pentoxyvérine
- Tipépidine
- Clopérastine
- Lévoloperastine
- Narceine , un alcaloïde de l'opium moins connu mais apparenté.
