Thiorédoxine - Thioredoxin
La thiorédoxine est une classe de petites protéines redox connues pour être présentes dans tous les organismes . Il joue un rôle dans de nombreux processus biologiques importants , y compris la signalisation redox. Chez l'homme, les thiorédoxines sont codées par les gènes TXN et TXN2 . La mutation par perte de fonction de l'un des deux gènes humains de la thiorédoxine est mortelle au stade de quatre cellules de l' embryon en développement . Bien qu'elle ne soit pas entièrement comprise, la thiorédoxine joue un rôle central chez l'homme et est de plus en plus liée à la médecine par sa réponse aux espèces réactives de l'oxygène (ROS). Chez les plantes , les thiorédoxines régulent un éventail de fonctions critiques, allant de la photosynthèse à la croissance, la floraison et le développement et la germination des graines. On a également découvert récemment qu'ils jouaient un rôle dans la communication de cellule à cellule .
Fonction
Les thiorédoxines sont des protéines qui agissent comme antioxydants en facilitant la réduction d'autres protéines par échange thiol-disulfure de cystéine . Les thiorédoxines se trouvent dans presque tous les organismes connus et sont essentielles à la vie des mammifères .
La thiorédoxine est une enzyme oxydoréductase de 12 kD contenant un site actif disulfure de dithiol. Il est omniprésent et présent dans de nombreux organismes, des plantes et des bactéries aux mammifères. De multiples substrats in vitro de la thiorédoxine ont été identifiés, notamment la ribonucléase , les choriogonadotrophines, les facteurs de coagulation, le récepteur des glucocorticoïdes et l'insuline. La réduction de l'insuline est classiquement utilisée comme test d'activité.
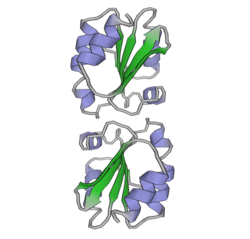
Les thiorédoxines sont caractérisées au niveau de leur séquence d' acides aminés par la présence de deux cystéines vicinales dans un motif CXXC . Ces deux cystéines sont la clé de la capacité de la thiorédoxine à réduire d'autres protéines. Les protéines de thiorédoxine ont également une structure tertiaire caractéristique appelée le repliement de la thiorédoxine .
Les thiorédoxines sont maintenues à l'état réduit par la flavoenzyme thiorédoxine réductase , dans une réaction NADPH-dépendante. Les thiorédoxines agissent comme donneurs d'électrons pour les peroxydases et la ribonucléotide réductase . Les glutarédoxines apparentées partagent de nombreuses fonctions des thiorédoxines, mais sont réduites par le glutathion plutôt que par une réductase spécifique.
L'avantage des thiorédoxines pour réduire le stress oxydatif est démontré par des souris transgéniques qui surexpriment la thiorédoxine, sont plus résistantes à l'inflammation et vivent 35 % plus longtemps, ce qui soutient la théorie du vieillissement des radicaux libres . Cependant, les témoins de cette étude étaient de courte durée, ce qui peut avoir contribué à l'augmentation apparente de la longévité. Trx1 peut réguler les modifications post-traductionnelles non redox. Chez les souris présentant une surexpression cardiaque spécifique de Trx1, l'étude protéomique a révélé que la protéine 1 contenant le domaine SET et MYND (SMYD1), une lysine méthyltransférase fortement exprimée dans les tissus cardiaques et autres tissus musculaires, est également régulée à la hausse. Cela suggère que Trx1 peut également jouer un rôle dans la méthylation des protéines via la régulation de l'expression de SMYD1, qui est indépendante de son activité oxydoréductase.
Les plantes ont un complément inhabituellement complexe de Trxs composé de six types bien définis (Trxs f, m, x, y, h et o) qui résident dans différents compartiments cellulaires et fonctionnent dans un éventail de processus. En 2010, il a été découvert pour la première fois que les protéines de la thiorédoxine sont capables de se déplacer d'une cellule à l'autre , ce qui représente une nouvelle forme de communication cellulaire chez les plantes.
Mécanisme d'action
La fonction principale de la thiorédoxine (Trx) est la réduction des résidus de cystéine oxydée et le clivage des liaisons disulfure. Pour Trx1, ce processus débute par attaque de Cys32, un des résidus conservés dans le motif thiorédoxine CXXC, sur le groupement oxydé du substrat. Presque immédiatement après cet événement Cys35, l'autre résidu Cys conservé dans Trx1, forme une liaison disulfure avec Cys32, transférant ainsi 2 électrons au substrat qui est maintenant sous sa forme réduite. Le Trx1 oxydé est ensuite réduit par la thiorédoxine réductase, qui à son tour est réduite par le NADPH comme décrit ci-dessus.
Interactions
Il a été démontré que la thiorédoxine interagit avec :
- ASK1 ,
- Collagène, type I, alpha 1 ,
- Récepteur des glucocorticoïdes ,
- SENP1 ,
- TXNIP .
- NF-κB - en réduisant une liaison disulfure dans NF-κB, Trx1 favorise la liaison de ce facteur de transcription à l'ADN.
- AP1 via Ref1 - Trx1 augmente indirectement l'activité de liaison à l'ADN de la protéine activatrice 1 (AP1) en réduisant le facteur redox 1 de l'enzyme de réparation de l' ADN (Ref-1), qui à son tour réduit AP1 dans un exemple de cascade de régulation redox.
- AMPK - La fonction AMPK dans les cardiomyocytes est préservée pendant le stress oxydatif en raison d'une interaction entre l'AMPK et Trx1. En formant un pont disulfure entre les deux protéines, Trx1 empêche la formation et l'agrégation d'AMPK oxydée, permettant ainsi à l'AMPK de fonctionner normalement et de participer aux cascades de signalisation .
Effet sur l'hypertrophie cardiaque
Il a été démontré que Trx1 régule négativement l'hypertrophie cardiaque , l'épaississement des parois des cavités cardiaques inférieures, par des interactions avec plusieurs cibles différentes. Trx1 régule positivement l'activité transcriptionnelle des facteurs respiratoires nucléaires 1 et 2 ( NRF1 et NRF2 ) et stimule l'expression du coactivateur 1-α du récepteur activé par les proliférateurs de peroxysomes 1-α ( PGC-1α ). De plus, Trx1 réduit deux résidus de cystéine dans l'histone désacétylase 4 ( HDAC4 ), ce qui permet à HDAC4 d'être importé du cytosol , où réside la forme oxydée, dans le noyau . Une fois dans le noyau, le HDAC4 réduit régule négativement l'activité des facteurs de transcription tels que le NFAT qui interviennent dans l'hypertrophie cardiaque. Trx 1 contrôle également les niveaux de microARN dans le cœur et s'est avéré inhiber l'hypertrophie cardiaque en régulant à la hausse miR-98 / let-7 . Trx1 peut réguler le niveau d'expression de SMYD1, ainsi peut moduler indirectement la méthylation des protéines à des fins de protection cardiaque.
La thiorédoxine dans les soins de la peau
La thiorédoxine est utilisée dans les produits de soins de la peau comme antioxydant en association avec la glutarédoxine et le glutathion.
Voir également
- RuBisCO - activité enzymatique régulée par la thiorédoxine
- Peroxiredoxine - activité enzymatique régulée par la thiorédoxine
- Pli de thiorédoxine
- Thiorédoxine réductase
Les références
Lectures complémentaires
- Arnér ES, Holmgren A (octobre 2000). « Fonctions physiologiques de la thiorédoxine et de la thiorédoxine réductase » . Journal Européen de Biochimie . 267 (20) : 6102-9. doi : 10.1046/j.1432-1327.2000.01701.x . PMID 11012661 .
- Nishinaka Y, Masutani H, Nakamura H, Yodoi J (2002). « Rôles régulateurs de la thiorédoxine dans les réponses cellulaires induites par le stress oxydatif ». Rapport d'oxydoréduction . 6 (5) : 289–95. doi : 10.1179/13510000001101536427 . PMID 11778846 . S2CID 34079507 .
- Ago T, Sadoshima J (novembre 2006). "Thioredoxine et remodelage ventriculaire" . Journal de cardiologie moléculaire et cellulaire . 41 (5) : 762-73. doi : 10.1016/j.yjmcc.2006.08.006 . PMC 1852508 . PMID 17007870 .
- Tonissen KF, Wells JR (juin 1991). « Isolement et caractérisation des gènes humains codant pour la thiorédoxine ». Gène . 102 (2) : 221–8. doi : 10.1016/0378-1119(91)90081-L . PMID 1874447 .
- Martin H, Dean M (février 1991). « Identification d'une protéine liée à la thiorédoxine associée aux membranes plasmiques ». Communications de recherche biochimique et biophysique . 175 (1) : 123-8. doi : 10.1016/S0006-291X(05)81209-4 . PMID 1998498 .
- Forman-Kay JD, Clore GM, Wingfield PT, Gronenborn AM (mars 1991). « Structure tridimensionnelle à haute résolution de la thiorédoxine humaine recombinante réduite en solution ». Biochimie . 30 (10) : 2685-98. doi : 10.1021/bi00224a017 . PMID 2001356 .
- Jacquot JP, de Lamotte F, Fontecave M, Schürmann P, Decottignies P, Miginiac-Maslow M, Wollman E (décembre 1990). « Relation de la réactivité de la thiorédoxine humaine-structure/fonction ». Communications de recherche biochimique et biophysique . 173 (3) : 1375-1381. doi : 10.1016/S0006-291X(05)80940-4 . PMID 2176490 .
- Forman-Kay JD, Clore GM, Driscoll PC, Wingfield P, Richards FM, Gronenborn AM (août 1989). « Une affectation de résonance magnétique nucléaire de proton et une détermination de la structure secondaire de la thiorédoxine humaine recombinante ». Biochimie . 28 (17) : 7088-97. doi : 10.1021/bi00443a045 . PMID 2684271 .
- Tagaya Y, Maeda Y, Mitsui A, Kondo N, Matsui H, Hamuro J, Brown N, Arai K, Yokota T, Wakasugi H (mars 1989). « Facteur dérivé de l'ATL (ADF), un récepteur IL-2/inducteur Tac homologue à la thiorédoxine ; implication possible de la réduction du dithiol dans l'induction du récepteur IL-2 » . Le Journal de l'EMBO . 8 (3) : 757-764. doi : 10.1002/j.1460-2075.1989.tb03436.x . PMC 400872 . PMID 2785919 .
- Wollman EE, d'Auriol L, Rimsky L, Shaw A, Jacquot JP, Wingfield P, Graber P, Dessarps F, Robin P, Galibert F (octobre 1988). "Clonage et expression d'un ADNc pour la thiorédoxine humaine" . Le Journal de Chimie Biologique . 263 (30) : 15506-12. doi : 10.1016/S0021-9258 (19) 37617-3 . PMID 3170595 .
- Heppell-Parton A, Cahn A, Bench A, Lowe N, Lehrach H, Zehetner G, Rabbitts P (mars 1995). « La thiorédoxine, un médiateur de l'inhibition de la croissance, correspond à 9q31 ». Génomique . 26 (2) : 379-81. doi : 10.1016/0888-7543 (95) 80223-9 . PMID 7601465 .
- Qin J, Clore GM, Kennedy WM, Huth JR, Gronenborn AM (mars 1995). « Structure de la solution de la thiorédoxine humaine dans un complexe intermédiaire disulfure mixte avec son peptide cible du facteur de transcription NF kappa B » . Structurer . 3 (3) : 289–97. doi : 10.1016/S0969-2126(01)00159-9 . PMID 7788295 .
- Kato S, Sekine S, Oh SW, Kim NS, Umezawa Y, Abe N, Yokoyama-Kobayashi M, Aoki T (décembre 1994). « Construction d'une banque d'ADNc humaine pleine longueur ». Gène . 150 (2) : 243–50. doi : 10.1016/0378-1119(94)90433-2 . PMID 7821789 .
- Qin J, Clore GM, Gronenborn AM (juin 1994). "Les structures de solution tridimensionnelles à haute résolution des états oxydés et réduits de la thiorédoxine humaine" . Structurer . 2 (6) : 503–22. doi : 10.1016/S0969-2126(00)00051-4 . PMID 7922028 .
- Gasdaska PY, Oblong JE, Cotgreave IA, Powis G (août 1994). « La séquence d'acides aminés prédite de la thiorédoxine humaine est identique à celle du facteur de croissance autocrine facteur dérivé des cellules T adultes (ADF) : l'ARNm de la thiorédoxine est élevé dans certaines tumeurs humaines ». Biochimica et Biophysica Acta (BBA) - Structure et expression des gènes . 1218 (3) : 292-6. doi : 10.1016/0167-4781(94)90180-5 . PMID 8049254 .
- Qin J, Clore GM, Kennedy WP, Kuszewski J, Gronenborn AM (mai 1996). "La structure en solution de la thiorédoxine humaine complexée avec sa cible de Ref-1 révèle une inversion de la chaîne peptidique" . Structurer . 4 (5) : 613-20. doi : 10.1016/S0969-2126(96)00065-2 . PMID 8736558 .
- Weichsel A, Gasdaska JR, Powis G, Montfort WR (juin 1996). « Structures cristallines des thiorédoxines humaines réduites, oxydées et mutées : preuve d'un homodimère réglementaire » . Structurer . 4 (6) : 735–51. doi : 10.1016/S0969-2126(96)00079-2 . PMID 8805557 .
- Andersen JF, Sanders DA, Gasdaska JR, Weichsel A, Powis G, Montfort WR (novembre 1997). « Homodimères de thiorédoxine humaine : régulation par le pH, rôle de l'aspartate 60 et structure cristalline de l'aspartate 60 --> mutant de l'asparagine ». Biochimie . 36 (46) : 13979-88. doi : 10.1021/bi971004s . PMID 9369469 .
- Maruyama T, Kitaoka Y, Sachi Y, Nakanoin K, Hirota K, Shiozawa T, Yoshimura Y, Fujii S, Yodoi J (novembre 1997). « Expression de la thiorédoxine dans l'endomètre humain pendant le cycle menstruel » . Reproduction Moléculaire Humaine . 3 (11) : 989-993. doi : 10.1093/molehr/3.11.989 . PMID 9433926 .
- Sahlin L, Stjernholm Y, Holmgren A, Ekman G, Eriksson H (décembre 1997). "L'expression de l'ARNm de la thiorédoxine est augmentée dans le col de l'utérus humain pendant la grossesse" . Reproduction Moléculaire Humaine . 3 (12) : 1113–7. doi : 10.1093/molehr/3.12.1113 . PMID 9464857 .
- Maeda K, Hägglund P, Finnie C, Svensson B, Henriksen A (novembre 2006). "Base structurelle pour la reconnaissance des protéines cibles par la protéine disulfure réductase thiorédoxine" . Structurer . 14 (11) : 1701–10. doi : 10.1016/j.str.2006.09.012 . PMID 17098195 .
Liens externes
- Thiorédoxine à la National Library of Medicine Medical Subject Headings (MeSH) des États-Unis
- Aperçu de toutes les informations structurelles disponibles dans le PDB pour UniProt : P10599 ( Thioredoxin ) au PDBe-KB .