Gertrude Maud Robinson - Gertrude Maud Robinson
Gertrude Maud Robinson | |
|---|---|
| Née |
Gertrude Maud Walsh
6 février 1886
Winsford , Cheshire
|
| Décédés | 1er mars 1954 (58 ans) |
| Nationalité | Anglais |
| Citoyenneté | Royaume-Uni |
| mère nourricière | Collège Owens |
| Conjoint(s) | Robert Robinson |
| Carrière scientifique | |
| Des champs | Chimie organique |
Gertrude Maud Robinson (anciennement Walsh) était une chimiste organique influente connue pour ses travaux sur les pigments végétaux ; le Piloty-Robinson Pyrrole Synthesis, qui porte son nom ; ses synthèses d' acides gras ; et sa synthèse de -hexénolactone, la première molécule synthétique ayant le caractère de la pénicilline .
Biographie
Robinson est née le 6 février 1886 à Winsford, Cheshire et est décédée d'une crise cardiaque le 1er mars 1954. Après avoir fréquenté l'école secondaire de Verdin , elle a obtenu son B. Sc. en 1907 et M. Sc. en 1908 du Collège Owens. Elle a ensuite fait des recherches à l'Université de Manchester sous la direction de Chaim Weizmann , qui est devenu plus tard le premier président d'Israël, et a enseigné la chimie au Manchester High School for Girls.
En 1912, elle épousa Robert Robinson , qui remporta plus tard le prix Nobel de 1947 et avec qui elle coécrivit de nombreux articles, et occupa le poste de démonstratrice non rémunérée à l' Université de Sydney avant de se rendre brièvement à St. Andrews en Écosse et à l' University College en Londres. Elle a travaillé sur les synthèses d'acides gras saturés et insaturés et a été la première à synthétiser l'acide oléique et l'acide lactarinique. Ses méthodes lui ont permis de synthétiser les acides gras ayant les plus grands poids moléculaires de l'époque (en particulier les acides tricontanoïque et 13-oxodotétracontanoïque).
Elle a également suggéré indépendamment la structure asymétrique des composés azoxy aromatiques et, avec son mari, a postulé un mécanisme pour la synthèse de l'indole de Fischer . Sur la base de ce mécanisme et à partir des synthèses de pyrrole de Piloty , le couple a proposé une méthode de synthèse du tétraphénylpyrrole. La synthèse de Pyrrole de Piloty-Robinson est nommée en leur honneur.
Après avoir déménagé à l' Université d'Oxford , Gertrude Robinson a commencé à étudier les pigments végétaux et a publié de nombreux articles sur les anthocyanes avec son mari. Elle a été la première à observer que la couleur du pigment d'une plante n'était pas liée au pH de sa sève et elle a été pionnière dans les travaux sur les leucoanthocyanes . De plus, elle a été la première à synthétiser la δ-hexénolactone, une molécule similaire à la pénicilline qui avait ses propriétés antibiotiques . En 1953, l'Université d'Oxford lui décerne une maîtrise honorifique .
Outre son travail de chimiste, Gertrude Robinson a eu deux enfants, Marion en 1921 et Michael en 1926. Elle était une passionnée d'alpinisme, une voyageuse prolifique et une hôtesse fréquente. Peut-être inspirant son travail sur les pigments végétaux, elle et son mari ont également entretenu un jardin pendant de nombreuses années.
Génétique végétale
Anthocyanes et copigments
Les fleurs, les fruits et les feuilles tirent leurs pigments des anthocyanes et des co- pigments (tels que les tanins et les flavonols ). Les combinaisons fournissent les couleurs exactes de diverses plantes à différents stades de développement. Les Robinson ont découvert qu'à différents rapports d'anthocyanes par rapport aux co-pigments, les co-pigments avaient des effets différents et ils ont postulé que cela était dû au fait que les co-pigments brisaient les complexes d'anthocyanes, qu'ils ont observés lorsqu'ils étaient en solution ensemble. Ils ont étudié ces pigments en comparant les distributions de couleurs dans des solutions non miscibles après des réactions avec des alcalis ou du chlorure ferrique .
Leucoanthocyanes
Les Robinson ont étudié la structure des leucoanthocyanines, des molécules incolores qui génèrent des anthocyanidines et sont présentes dans la plupart des plantes. Rosenheim a découvert simultanément les leucoanthocyanes et il a inventé le terme. Les leucoanthocyanines sont présentes dans plus d'endroits (bois, écorce, coquilles de noix, fleurs, fruits) que les anthocyanes normales.
Synthèse de Pyrrole de Piloty-Robinson
Cette réaction, initialement nommée d'après Piloty, a reçu le nom de Robinson en raison de leur travail sur le mécanisme. Bien qu'il ne soit pas clair de quel Robinson la synthèse porte le nom technique, l'article sur le sujet a été rédigé par Gertrude et Robert.
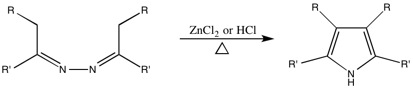
Synthèse généralisée
Cette réaction est utilisée pour convertir les azines en pyrroles 3,4-disubstitués.
Mécanisme généralisé
Le mécanisme tel que suggéré par les Robinson.
Il y a cependant quelques problèmes avec certaines synthèses. La réaction de Piloty-Robinson entre en compétition avec la formation de pyrazoline lorsque le réactif est une azine aliphatique dérivée d'une cétone. De plus, sous des températures élevées et des solutions très acides, les azines dérivées d'aldéhydes ne sont pas stables. Cela empêche la formation de pyrroles 2,5-disubstitués (où R = H) en utilisant cette méthode.
Utilisations modernes
Si les pyrroles produits par la synthèse de Piloty-Robinson sont souvent très utiles, la réaction elle-même n'est pas toujours favorable car elle nécessite des températures élevées et des temps de réaction longs en plus des problèmes évoqués ci-dessus, le rendement est souvent faible ou modéré. Les méthodes modernes ont atténué certaines de ces préoccupations.
Irradiation par micro-ondes
Le rayonnement micro-ondes réduit le temps nécessaire à la réaction d'environ 3 jours à 30-60 min. Cela peut également affecter le rendement.
Solidement pris en charge
Les synthèses sur support solide offrent un traitement et une purification plus faciles et plus efficaces.
Mécanisme Fischer Indole
Les Robinson ont réfuté bon nombre des théories dominantes sur le mécanisme de l'indole de Fischer en montrant que la réaction n'était pas perturbée en présence d'autres amines aromatiques telles que la p- toluidine . C'est le mécanisme qu'ils ont suggéré (où les déplacements d'hydrogène peuvent également être interprétés comme des échanges d'hydrogène dans l'acide).
Acides gras saturés et insaturés
Méthodes de synthèse des acides gras supérieurs
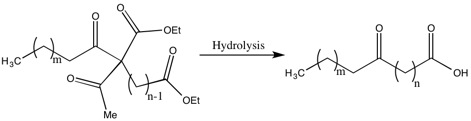
Un des inconvénients des méthodes de Robinsons pour la synthèse des acides gras sont les faibles rendements dus aux récupérations d'une partie importante du dialdéhyde. La justification par Gertrude Robinson de ce faible rendement était que l' aldéhyde intermédiaire était un acide plus faible que l'acide acétique , qui a été éliminé au cours d'une étape de l'hydrolyse. Si elle n'a pas résolu ce problème, elle a amélioré le rendement et diminué le dialdéhyde récupéré par « l'acylation d'un acétoacétate d'éthyle substitué par le groupe apparenté à l'acide le plus faible possible ».
Un exemple en est la synthèse de l'acide 10-cétotridécoïque via l'acide 13-dicétopalmitique, qui est un acide important car, avec la réduction et la déshydratation, il devient la molécule qui est une hormone ovarienne active.
Gertrude Robinson, en utilisant ses méthodes de synthèse d'acides gras supérieurs, a synthétisé l' acide n-triacontanoïque , également connu sous le nom d'acide mélissique, et l'acide 13-oxodotétracontanoïque.
L'acide oléique
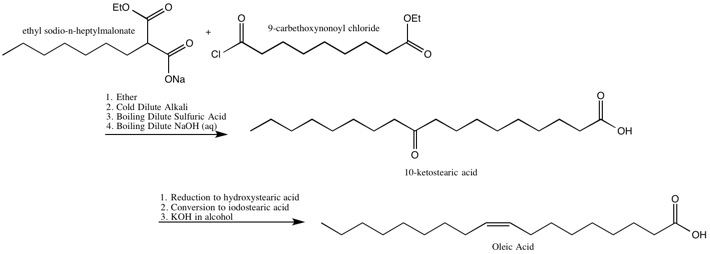
Les Robinson ont identifié l'emplacement de la double liaison dans l'acide oléique et l'ont également synthétisé .
La synthèse de Robinsons de l'acide oléique
Acide lactarinique
L'acide lactarinique, isolé des champignons du genre Lactarius , s'est avéré contenir un acide cétostéarique. Les Robinson ont montré qu'il s'agissait en fait d'acide 6-cétostéarique en effectuant une transformation de Beckmann sur l' oxime de l'acide lactarinique. Ils ont ensuite synthétisé l'acide 6-cétostéarique via une réaction de sodio-2-acétyl-n-tridécoate d'éthyle et de chlorure de 5-carbéthoxyvaléryle, puis hydrolyse pour prouver la structure de l'acide lactarinique.