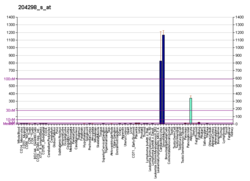
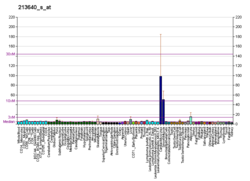
Lysyl oxydase - Lysyl oxidase
La lysyl oxydase ( LOX ), également connue sous le nom de protéine-lysine 6-oxydase , est une enzyme qui, chez l'homme, est codée par le gène LOX . Il catalyse la conversion des molécules de lysine en aldéhydes hautement réactifs qui forment des liaisons croisées dans les protéines de la matrice extracellulaire . Son inhibition peut provoquer un ostéolathyrisme , mais, en même temps, sa régulation positive par les cellules tumorales peut favoriser la métastase de la tumeur existante, la rendant maligne et cancéreuse .
Structure
Dans la souche de levure Pichia pastoris , la lysyl oxydase constitue une structure homodimérique . Chaque monomère est constitué d'un site actif qui comprend un atome de Cu(II) coordonné avec trois résidus histidine ainsi que la 2,4,5-trihydroxyphénalanine quinone (TPQ), un cofacteur crucial .
Chez l'homme, le gène LOX est localisé sur le chromosome 5 q23.3-31.2. La séquence d'ADN code pour un polypeptide de 417 acides aminés dont les 21 premiers résidus constituent un peptide signal, d'un poids d'environ 32 kDa. L'extrémité carboxy contient l'ion cuivre (II) actif, les résidus lysine, tyrosine et cystéine qui constituent le site catalytiquement actif. La structure tridimensionnelle de la lysyl oxydase humaine n'a pas encore été résolue.
Mécanisme
| protéine-lysine 6-oxydase | |||||||||
|---|---|---|---|---|---|---|---|---|---|
 Mécanisme Lox
| |||||||||
| Identifiants | |||||||||
| CE n° | 1.4.3.13 | ||||||||
| N ° CAS. | 99676-44-5 | ||||||||
| Bases de données | |||||||||
| IntEnz | Vue IntEnz | ||||||||
| BRENDA | Entrée BRENDA | ||||||||
| ExPASy | Vue NiceZyme | ||||||||
| KEGG | Entrée KEGG | ||||||||
| MétaCycle | voie métabolique | ||||||||
| PRIAM | profil | ||||||||
| Structures de l' APB | RCSB PDB PDBe PDBsum | ||||||||
| Ontologie des gènes | AmiGO / QuickGO | ||||||||
| |||||||||
Le mécanisme de la lysyl oxydase se produit via la modification du groupe -amino d'une chaîne latérale de lysine . L'enzyme appartient à la catégorie des amines oxydases de cuivre contenant de la quinone , et la réaction dépend fortement du cofacteur lysyl tyrosylquinone (LTQ). Le cofacteur LTQ est unique parmi les quinones en raison de sa structure ortho/benzoquinone et de sa charge neutre à pH physiologique. Cela peut être mis en contraste avec le quinocofacteur TPQ omniprésent similaire, qui existe sous forme de structure chargée négativement dans des conditions physiologiques et comprend une fonctionnalité de résonance ortho/para-carbonyle.
La LTQ est cruciale dans la conversion catalysée par LOX des résidus de lysine en -aminoadipidic-δ-semialdéhydes, généralement appelés allysines . Dans l'oxydation de la lysine, l'-amine est d'abord convertie en une base de Schiff par réaction avec la LTQ. Alors que la LTQ est toujours liée au substrat, l'élimination limitante du proton produit un intermédiaire imine. L'hydrolyse subséquente de l'imine conduit à la libération du produit aldéhyde, l'allysine. L'oxygène moléculaire et l'ion cuivre sont utilisés pour réoxyder le cofacteur et produire une autre imine, produisant du peroxyde d'hydrogène comme produit secondaire. Une hydrolyse supplémentaire libère de l'ammoniac et le cofacteur d'origine, complétant ainsi le cycle catalytique.
Fonction biologique
La lysyl oxydase est une enzyme extracellulaire dépendante du cuivre qui catalyse la formation d'aldéhydes à partir de résidus de lysine dans les précurseurs de collagène et d' élastine . Ces aldéhydes sont hautement réactifs et subissent des réactions chimiques spontanées avec d'autres résidus aldéhydes dérivés de la lysyl oxydase, ou avec des résidus lysine non modifiés. Il en résulte une réticulation du collagène et de l'élastine, ce qui est essentiel pour la stabilisation des fibrilles de collagène et pour l'intégrité et l'élasticité de l'élastine mature.
Des liaisons croisées complexes se forment dans le collagène ( pyridinolines dérivées de trois résidus lysine) et dans l'élastine ( desmosines dérivées de quatre résidus lysine) qui diffèrent par leur structure.
L'importance de la réticulation dérivée de la lysyl oxydase a été établie à partir d'études animales dans lesquelles la lysyl oxydase était inhibée soit par une carence nutritionnelle en cuivre, soit par la supplémentation des régimes alimentaires en -aminopropionitrile (BAPN), un inhibiteur de la lysyl oxydase. Cela a entraîné un lathyrisme , caractérisé par une formation et une résistance osseuses médiocres, une peau hyperextensible, des ligaments faibles et une augmentation de la fréquence des anévrismes aortiques . Ces anomalies étaient bien corrélées avec une diminution de la réticulation du collagène et de l'élastine.
Au cours du développement, des niveaux réduits de lysyl oxydase ont été impliqués dans la maladie de Menkes et le syndrome de la corne occipitale , deux troubles récessifs liés à l'X caractérisés par une mutation dans un gène de transport du cuivre. Ainsi, non seulement la LOX est cruciale pour le développement cardiovasculaire, mais on pense qu'elle joue un rôle majeur dans le développement du tissu conjonctif et peut également être importante dans la fonction neurologique.
La lysyl oxydase s'est également avérée cruciale pour le développement du système respiratoire et de la peau, car le collagène et l'élastine représentent 50 à 60 % de la composition du poumon et 75 % de la peau. Dans les modèles à double knock-out LOX ( Lox -/- ), la fonction de LOX a été réduite jusqu'à 80 %, et le phénotype des poumons ressemble à celui des patients humains souffrant d' emphysème et de voies respiratoires distales dilatées.
Enfin, la lysyl oxydase joue un rôle crucial dans l'étape d'engagement de la formation des adipocytes , ou cellules graisseuses, à partir des cellules souches pluripotentes au cours du développement. Son absence peut conduire à des défauts dans la superfamille bêta du facteur de croissance transformant des protéines, qui contrôlent la croissance et la différenciation cellulaires .
Signification clinique
L'expression de LOX est régulée par des facteurs inductibles par l' hypoxie (HIF) et, par conséquent, l'expression de LOX est souvent régulée à la hausse dans les tumeurs hypoxiques du sein et de la tête et du cou. Les patients présentant des tumeurs à haute expression de LOX ont une faible survie globale. De plus, il a été démontré que l'inhibition de LOX élimine les métastases chez la souris. La LOX sécrétée est responsable des propriétés invasives des cellules cancéreuses hypoxiques par le biais de l' activité kinase d'adhésion focale et de l'adhésion cellule-matrice. LOX peut être nécessaire pour créer une niche permissive pour la croissance métastatique et, ainsi, peut être nécessaire pour les métastases induites par l'hypoxie. En fait, des recherches récentes ont montré que la surexpression de LOX est cruciale pour favoriser la croissance tumorale et les métastases dans plusieurs cancers, notamment le cancer du sein, le cancer du poumon non à petites cellules et le cancer colorectal.
L'expression de LOX a également été détectée dans les mégacaryocytes, ou cellules de la moelle osseuse responsables de la production de plaquettes. Les données dérivées d'un modèle murin de myélofibrose impliquaient LOX dans la fibrose de la moelle osseuse.
Dans un modèle de cancer du sein chez le rongeur, une petite molécule ou un anticorps inhibiteur de LOX a aboli les métastases. La LOX sécrétée par les cellules tumorales hypoxiques du sein réticule le collagène dans la membrane basale et est essentielle au recrutement des cellules myéloïdes CD11b+ . Les cellules CD11b+ adhèrent à leur tour au collagène réticulé et produisent la métalloprotéinase-2 matricielle , qui clive le collagène, favorisant l'invasion des cellules tumorales métastasantes. En revanche, l'inhibition de LOX empêche le recrutement des cellules CD11b+ et la croissance métastatique.
Dans les cellules dépourvues de récepteurs du TGF-β, un déficit caractéristique du cancer du poumon , la lysyl oxydase est retrouvée à des concentrations élevées. L'immunocoloration LOX a révélé qu'une expression élevée de LOX est associée à une grande invasion de carcinome dans des échantillons obtenus à partir d' adénocarcinomes pulmonaires prélevés chirurgicalement . De plus, l'expression de LOX est un indicateur de survie à 5 ans chez les patients, avec une chance de survie de 71 % pour les patients ayant des niveaux de LOX faibles, contre 43 % pour les patients ayant des niveaux de LOX élevés. Ainsi, la régulation à la hausse de la lysyl oxydase est un prédicteur de mauvais pronostic chez les patients atteints d'adénocarcinome à un stade précoce.
La lysyl oxydase a été récemment impliquée dans l' angiogenèse tumorale ou la formation de vaisseaux sanguins , à la fois in vivo et in vitro . Il a été démontré que la LOX dérivée d'une tumeur sous-cutanée augmentait l' expression et la sécrétion du facteur de croissance endothélial vasculaire (VEGF), ce qui favorise ensuite l'angiogenèse par phosphorylation de la protéine kinase B , ou Akt, via le récepteur du facteur de croissance dérivé des plaquettes β ( PDGFRB ). Des niveaux élevés de LOX ont été associés à une densité élevée des vaisseaux sanguins dans les échantillons de patients. Les inhibiteurs LOX cliniquement pertinents peuvent aider à ralentir la progression du cancer en régulant à la baisse les facteurs de croissance cruciaux qui favorisent la progression des tumeurs solides.
Par conséquent, les inhibiteurs de l'enzyme LOX peuvent être utiles pour prévenir l'angiogenèse, la progression tumorale et les métastases ainsi que traiter d'autres maladies fibrotiques impliquant le remodelage de la matrice extracellulaire , y compris les maladies neurodégénératives et cardiovasculaires.
Voir également
Les références
Lectures complémentaires
- Csiszar K (2001). Lysyl oxydases : une nouvelle famille d'amines oxydases multifonctionnelles . Progrès dans la recherche sur les acides nucléiques et la biologie moléculaire. 70 . p. 1–32. doi : 10.1016/S0079-6603(01)70012-8 . ISBN 9780125400701. PMID 11642359 .
- Kagan HM, Li W (mars 2003). « Lysyl oxydase : propriétés, spécificité et rôles biologiques à l'intérieur et à l'extérieur de la cellule ». Journal de biochimie cellulaire . 88 (4) : 660-72. doi : 10.1002/jcb.10413 . PMID 12577300 . S2CID 23651213 .
- Svinarich DM, Twomey TA, Macauley SP, Krebs CJ, Yang TP, Krawetz SA (juillet 1992). "Caractérisation du locus du gène de la lysyl oxydase humaine" . Le Journal de Chimie Biologique . 267 (20) : 14382-7. doi : 10.1016/S0021-9258 (19) 49723-8 . PMID 1352776 .
- Mariani TJ, Trackman PC, Kagan HM, Eddy RL, Shows TB, Boyd CD, Deak SB (juin 1992). « La séquence d'acides aminés dérivée complète de la lysyl oxydase humaine et l'affectation du gène au chromosome 5 (homologie de séquence étendue avec le gène de résolution ras murin) ». Matrice . 12 (3) : 242–8. doi : 10.1016/S0934-8832(11)80067-3 . PMID 1357535 .
- Murawaki Y, Kusakabe Y, Hirayama C (décembre 1991). « Activité lysyl oxydase sérique dans les maladies chroniques du foie par rapport aux taux sériques de prolyl hydroxylase et de laminine ». Hépatologie . 14 (6) : 1167-1173. doi : 10.1002/hep.1840140635 . PMID 1683640 . S2CID 25820738 .
- Hämäläinen ER, Jones TA, Sheer D, Taskinen K, Pihlajaniemi T, Kivirikko KI (novembre 1991). « Clonage moléculaire de la lysyl oxydase humaine et affectation du gène au chromosome 5q23.3-31.2 ». Génomique . 11 (3) : 508–16. doi : 10.1016/0888-7543(91)90057-L . PMID 1685472 .
- Konishi A, Iguchi H, Ochi J, Kinoshita R, Miura K, Uchino H (octobre 1985). « Augmentation de l'activité lysyl oxydase dans le milieu de culture de cellules non parenchymateuses de foies fibrotiques ». Gastro-entérologie . 89 (4) : 709–15. doi : 10.1016/0016-5085(85)90563-3 . PMID 2863189 .
- Kuivaniemi H, Ala-Kokko L, Kivirikko KI (septembre 1986). « Sécrétion de lysyl oxydase par des fibroblastes cutanés humains cultivés et effets de la monensine, de la nigéricine, de la tunicamycine et de la colchicine ». Biochimica et Biophysica Acta (BBA) - Sujets généraux . 883 (2) : 326–34. doi : 10.1016/0304-4165(86)90325-9 . PMID 2874833 .
- Reiser KM, Hennessy SM, Last JA (déc. 1987). « Analyse des changements associés à l'âge dans la réticulation du collagène dans la peau et les poumons chez les singes et les rats ». Biochimica et Biophysica Acta (BBA) - Sujets généraux . 926 (3) : 339–48. doi : 10.1016/0304-4165(87)90220-0 . PMID 3120785 .
- Järveläinen H, Halme T, Rönnemaa T (1982). « Effet du cortisol sur la prolifération et la synthèse des protéines des cellules musculaires lisses aortiques humaines en culture ». Acta Medica Scandinavica. Supplément . 660 : 114–22. doi : 10.1111/j.0954-6820.1982.tb00367.x . PMID 6127904 .
- Kuivaniemi H, Savolainen ER, Kivirikko KI (juin 1984). "Lysyl oxydase placentaire humaine. Purification, caractérisation partielle et préparation de deux antisérums spécifiques à l'enzyme" . Le Journal de Chimie Biologique . 259 (11) : 6996–7002. doi : 10.1016/S0021-9258 (17) 39828-9 . PMID 6144680 .
- Lien YH, Stern R, Fu JC, Siegel RC (septembre 1984). « Inhibition de la formation de fibrilles de collagène in vitro et réticulation ultérieure par le glucose ». Sciences . 225 (4669) : 1489-1491. doi : 10.1126/science.6147899 . PMID 6147899 .
- Yasutake A, Powers JC (juin 1981). "Réactivité de l'élastase leucocytaire humaine et de l'élastase pancréatique porcine envers les peptides 4-nitroanilides contenant des résidus modèles de desmosine. Preuve que l'élastase leucocytaire humaine est sélective pour les régions réticulées d'élastine". Biochimie . 20 (13) : 3675–9. doi : 10.1021/bi00516a002 . PMID 6912069 .
- Kim Y, Boyd CD, Csiszar K (mars 1995). « Un nouveau gène avec une séquence et une similarité structurelle avec le gène codant pour la lysyl oxydase humaine » . Le Journal de Chimie Biologique . 270 (13) : 7176–82. doi : 10.1074/jbc.270.13.7176 . PMID 7706256 .
- Hämäläinen ER, Kemppainen R, Pihlajaniemi T, Kivirikko KI (septembre 1993). « Structure du gène de la lysyl oxydase humaine ». Génomique . 17 (3) : 544–8. doi : 10.1006/geno.1993.1369 . PMID 7902322 .
- Forbes EG, Cronshaw AD, MacBeath JR, Hulmes DJ (septembre 1994). "La protéine de matrice acide riche en tyrosine (TRAMP) est une protéine tyrosine-sulfatée et largement distribuée de la matrice extracellulaire" . Lettres FEBS . 351 (3) : 433-6. doi : 10.1016/0014-5793(94)00907-4 . PMID 8082810 . S2CID 23360856 .
- Csiszar K, Mariani TJ, Gosin JS, Deak SB, Boyd CD (mai 1993). « Un polymorphisme de longueur de fragment de restriction entraîne une substitution d'acides aminés non conservatrice codée dans le premier exon du gène de la lysyl oxydase humaine ». Génomique . 16 (2) : 401-6. doi : 10.1006/geno.1993.1203 . PMID 8100215 .
- Vetter U, Weis MA, Mörike M, Eanes ED, Eyre DR (février 1993). « Les liaisons croisées du collagène et la cristallinité minérale dans l'os des patients atteints d'ostéogenèse imparfaite ». Journal de recherche sur les os et les minéraux . 8 (2) : 133-7. doi : 10.1002/jbmr.5650080203 . PMID 8442432 . S2CID 21904627 .
- Panchenko MV, Stetler-Stevenson WG, Trubetskoy OV, Gacheru SN, Kagan HM (mars 1996). "Activité métalloprotéinase sécrétée par les cellules fibrogènes dans le traitement de la prolysyl oxydase. Rôle potentiel de la procollagène C-protéinase" . Le Journal de Chimie Biologique . 271 (12) : 7113-9. doi : 10.1074/jbc.271.12.7113 . PMID 8636146 .
- Khakoo A, Thomas R, Trompeter R, Duffy P, Price R, Pope FM (février 1997). « Déficit congénital de la cutis laxa et de la lysyl oxydase ». Génétique Clinique . 51 (2) : 109-14. doi : 10.1111/j.1399-0004.1997.tb02430.x . PMID 9111998 . S2CID 36246895 .
- Smithen DA, Leung LM, Challinor M, Lawrence R, Tang H, Niculescu-Duvaz D, et al. (mars 2020). "Les inhibiteurs du 2-aminométhylène-5-sulfonylthiazole de la lysyl oxydase (LOX) et du LOXL2 montrent une efficacité significative pour retarder la croissance tumorale" . Journal de chimie médicinale . 63 (5) : 2308–2324. doi : 10.1021/acs.jmedchem.9b01112 . PMC 7073924 . PMID 31430136 .
Liens externes
- Lysyl+Oxidase à la National Library of Medicine Medical Subject Headings (MeSH) des États-Unis