Ligand non innocent - Non-innocent ligand
En chimie , un ligand (redox) non innocent est un ligand dans un complexe métallique où l'état d'oxydation n'est pas clair. En règle générale, les complexes contenant des ligands non innocents sont redox actifs à des potentiels légers . Le concept suppose que les réactions redox dans les complexes métalliques sont localisées en métal ou en ligand, ce qui est une simplification, quoique utile.
CK Jørgensen a d'abord décrit les ligands comme "innocents" et "suspects": "Les ligands sont innocents lorsqu'ils permettent de définir les états d'oxydation des atomes centraux. Le cas le plus simple d'un ligand suspect est NON ..."
Réactions redox des complexes de ligands innocents et non innocents
Classiquement, les réactions redox des complexes de coordination sont supposées être centrées sur le métal. La réduction de MnO 4 - en MnO 4 2− est décrite par le changement de l'état d'oxydation du manganèse de 7+ à 6+. Les ligands oxydes ne changent pas à l'état d'oxydation, restant 2-. L'oxyde est un ligand innocent. Un autre exemple de métal centré classique couple redox est [Co (NH 3 ) 6 ] 3+ / [Co (NH 3 ) 6 ] 2+ . L'ammoniac est innocent dans cette transformation.
Le comportement redox non innocent des ligands est illustré par le nickel bis (stilbènedithiolate) ([Ni (S 2 C 2 Ph 2 ) 2 ] z ). Comme tous les complexes bis (1,2-dithiolène) de n d 8 ions métalliques, trois états d'oxydation peuvent être identifiés: z = 2-, 1- et 0. Si les ligands sont toujours considérés comme dianioniques (comme cela est fait dans comptage de l'état d'oxydation formel), alors z = 0 exige que le nickel ait un état d'oxydation formel de + IV. L' état d'oxydation formel de l'atome central de nickel varie donc de + II à + IV dans les transformations ci-dessus (voir figure). Cependant, l'état d'oxydation formel est différent de l'état d'oxydation réel (spectroscopique) basé sur la configuration (spectroscopique) des électrons-d métalliques. Le stilbène-1,2-dithiolate se comporte comme un ligand redox non innocent, et les processus d'oxydation se déroulent en fait au niveau des ligands plutôt que du métal. Cela conduit à la formation de complexes radicaux ligand. Le complexe de charge neutre (z = 0), présentant un caractère diradical singulet partiel, est donc mieux décrit comme un dérivé Ni 2+ de l'anion radical S 2 C 2 Ph 2 • - . Le diamagnétisme de ce complexe provient du couplage antiferromagnétique entre les électrons non appariés des deux radicaux ligands. Un autre exemple est les états d'oxydation plus élevés des complexes de cuivre de ligands diamido phényl qui sont stabilisés par une liaison hydrogène multicentrique intramoléculaire.
Ligands non innocents typiques
- Le nitrosyl (NO) se lie aux métaux dans l'une des deux géométries extrêmes - plié où NO est traité comme un pseudohalogénure (NO - ) et linéaire, où NO est traité comme NO + .
- Le dioxygène peut être non innocent, car il existe dans deux états d'oxydation, le superoxyde (O 2 - ) et le peroxyde (O 2 2− ).
Ligands à délocalisation pi étendue tels que porphyrines , phtalocyanines et corroles et ligands de formules généralisées [D-CR = CR-D] n- (D = O, S, NR 'et R, R' = alkyle ou aryle ) sont souvent non innocents. En revanche, [D-CR = CR-CR = D] - tels que NacNac ou acac sont innocents.
- catécholates et 1,2-dioxalènes apparentés.
- les dithiolènes , tels que le maléonitrilédithiolate (voir l'exemple de [Ni (S 2 C 2 Ph 2 ) 2 ] n− ci-dessus).
- Les 1,2- diimines tels que les dérivés du 1,2-diamidobenzène, de la 2,2'-bipyridine et du diméthylglyoxime . Le complexe Cr ( 2,2'-bipyridine ) 3 est un dérivé de Cr (III) lié à trois ligands bipyridine 1− . D'autre part, l'oxydation à un électron de [Ru (2,2'-bipyridine) 3 ] 2+ est localisée sur Ru et la bipyridine se comporte comme un ligand normal et innocent dans ce cas.
- les ligands contenant du ferrocène peuvent avoir des événements d'oxydation centrés sur le centre du fer ferrocène plutôt que sur le centre du métal catalytiquement actif.
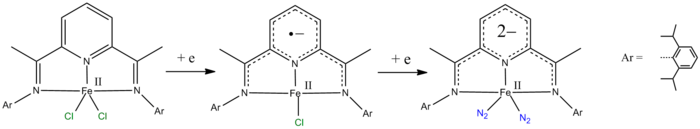
- Les ligands pyridine-2,6-diimine peuvent être réduits d'un et deux électrons.
Ligands redox non innocents en biologie et catalyse homogène
Dans certains processus enzymatiques, les cofacteurs redox non innocents fournissent des équivalents redox pour compléter les propriétés redox des métalloenzymes. Bien entendu, la plupart des réactions redox dans la nature impliquent des systèmes innocents, par exemple des clusters [4Fe-4S] . Les équivalents redox supplémentaires fournis par les ligands redox non innocents sont également utilisés comme facteurs de contrôle pour diriger la catalyse homogène.
Hèmes

Les ligands de la porphyrine peuvent être innocents (2-) ou non innocents (1-). En enzymes chloroperoxydase et le cytochrome P450 , le ligand porphyrine sustains oxydation au cours du cycle catalytique, en particulier dans la formation du composé I . Dans d'autres protéines hème , telles que la myoglobine , l'oxydoréduction centrée sur le ligand ne se produit pas et la porphyrine est innocente.
Galactose oxydase
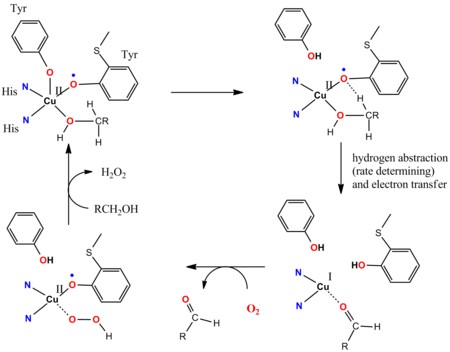
Le cycle catalytique de la galactose oxydase (GOase) illustre l'implication de ligands non innocents. La GOase oxyde les alcools primaires en aldéhydes en utilisant O 2 et en libérant H 2 O 2 . Le site actif de l'enzyme GOase comporte un tyrosyle coordonné à un ion Cu II . Dans les étapes clés du cycle catalytique, un site de ligand basique Brønsted coopératif déprotone l'alcool, et par la suite l'atome d'oxygène du radical tyrosinyle soustrait un atome d'hydrogène de la fonctionnalité alpha-CH du substrat d'alcoxyde coordonné. Le radical tyrosinyle participe au cycle catalytique: la 1e-oxydation est effectuée par le couple Cu (II / I) et l'oxydation 1e est effectuée par le radical tyrosyle, ce qui donne un 2e changement global. L'abstraction radicale est rapide. Le couplage antiferromagnétique entre les spins non appariés du ligand radical tyrosine et le centre d 9 Cu II donne lieu à l'état fondamental diamagnétique, cohérent avec les modèles synthétiques.
Voir également
Les références
- ^ Ganguly, Sumit; Ghosh, Abhik (16/07/2019). "Sept indices à Ligand Noninnocence: Le Paradigme de Metallocorrole". Comptes de la recherche chimique . 52 (7): 2003-2014. doi : 10.1021 / acs.accounts.9b00115 . ISSN 0001-4842 . PMID 31243969 .
- ^ Jørgensen CK (1966). "Les différences entre les quatre ligands halogénure, et les remarques de discussion sur les complexes trigonaux-bipyramidaux, sur les états d'oxydation et sur les éléments diagonaux de l'énergie à un électron". Examens de chimie de coordination . 1 (1–2): 164–178. doi : 10.1016 / S0010-8545 (00) 80170-8 .
- ^ Bien qu'un examen plus attentif de la structure électronique des partenaires redox révèle cependant que les ligands oxydes sont affectés par le changement redox, cet effet est mineur et l'état d'oxydation formel de l'oxygène reste le même.
- ^ Aragoni, M. Carla; Caltagirone, Claudia; Lippolis, Vito; Podda, Enrico; Slawin, Alexandra MZ; Woollins, J. Derek; Pintus, Anna; Arca, Massimiliano (07/12/2020). "Caractère diradical des complexes métalliques de bis (1,2-dithiolène) hétéroleptiques neutres: étude de cas de [Pd (Me2timdt) (mnt)] (Me2timdt = 1,3-diméthyl-2,4,5-trithioxoimidazolidine; mnt2– = 1 , 2-dicyano-1,2-éthylènedithiolate) " . Chimie inorganique . 59 (23): 17385–17401. doi : 10.1021 / acs.inorgchem.0c02696 . ISSN 0020-1669 . PMC 7735710 . PMID 33185438 .
- ^ Rajabimoghadam, Khashayar; Darwish, Yousef; Bashir, Umyeena; Pitman, Dylan; Eichelberger, Sidney; Siegler, Maxime A .; Swart, Marcel; Garcia-Bosch, Isaac (2018). "Oxydation aérobie catalytique d'alcools par des complexes de cuivre portant des ligands redox-actifs avec des groupes de liaison H accordables" . Journal de l'American Chemical Society . 140 (48): 16625-16634. doi : 10.1021 / jacs.8b08748 . PMC 6645702 . PMID 30400740 .
- ^ Kaim W, Schwederski B (2010). "Ligands non-innocents dans la chimie bioinorganique - Un aperçu". Examens de chimie de coordination . 254. (13-14) (13-14): 1580-1588. doi : 10.1016 / j.ccr.2010.01.009 .
- ^ Ghosh, Abhik (22/02/2017). "Structure électronique des dérivés de corrole: aperçus des structures moléculaires, spectroscopie, électrochimie et calculs chimiques quantiques". Examens chimiques . 117 (4): 3798–3881. doi : 10.1021 / acs.chemrev.6b00590 . ISSN 0009-2665 .
- ^ Zanello P, Corsini M (2006). "Complexes de métaux de transition homoleptiques et mononucléaires de 1,2-dioxolènes: mise à jour de leurs propriétés électrochimiques à structurelles (rayons X)". Examens de chimie de coordination . 250 (15–16): 2000–2022. doi : 10.1016 / j.ccr.2005.12.017 .
- ^ Wang X, Thevenon A, Brosmer JL, Yu I, Khan SI, Mehrkhodavandi P, Diaconescu PL (août 2014). "Contrôle redox de l'activité de polymérisation par ouverture de cycle métallique du groupe 4 vers le L-lactide et l'ε-caprolactone" . Confiture. Chem. Soc . 136 (32): 11264–7. doi : 10.1021 / ja505883u . PMID 25062499 .
- ^ de Bruin B, Bill E, Bothe E, Weyhermüller T, Wieghardt K (juin 2000). "Structures moléculaires et électroniques de complexes métalliques bis (pyridine-2,6-diimine) [ML2] (PF6) n (n & # 61; 0, 1, 2, 3; M & # 61; Mn, Fe, Co, Ni, Cu, Zn) ". Inorg Chem . 39 (13): 2936–47. doi : 10.1021 / ic000113j . PMID 11232835 .
- ^ Chirik PJ, Wieghardt K (février 2010). "Chimie. Les ligands radicaux confèrent la noblesse aux catalyseurs en métal de base". La science . 327 (5967): 794–5. doi : 10.1126 / science.1183281 . PMID 20150476 .
- ^ Lyaskovskyy V, de Bruin B (2012). "Redox Non-Innocent Ligands: Nouveaux outils polyvalents pour contrôler les réactions catalytiques". Catalyse ACS . 2 (2): 270-279. doi : 10.1021 / cs200660v .
- ^ Luca OR, Crabtree RH (février 2013). "Ligands Redox-actifs dans la catalyse". Chem Soc Rev . 42 (4): 1440–59. doi : 10.1039 / c2cs35228a . PMID 22975722 .
- ^ Chirila, Andrei; Das, Braja Gopal; Kuijpers, Petrus F .; Sinha, Vivek; Bruin, Bas de (2018), "Application of Stimuli-Responsive and" Non-innocent "Ligands in Base Metal Catalysis", Non-Noble Metal Catalysis , John Wiley & Sons, Ltd, pp. 1–31, doi : 10.1002 / 9783527699087.ch1 , ISBN 9783527699087
- ^ Whittaker MM, Whittaker JW (mars 1993). "Interactions de ligand avec la galactose oxydase: aperçus mécanistes" . Biophys. J . 64 (3): 762–72. Bibcode : 1993BpJ .... 64..762W . doi : 10.1016 / S0006-3495 (93) 81437-1 . PMC 1262390 . PMID 8386015 .
- ^ Wang Y, DuBois JL, Hedman B, Hodgson KO, Stack TD (janvier 1998). "Modèles catalytiques de galactose oxydase: réactivité biomimétique du radical Cu (II) -phenoxyl". La science . 279 (5350): 537–40. Bibcode : 1998Sci ... 279..537W . doi : 10.1126 / science.279.5350.537 . PMID 9438841 .
- ^ Müller J, Weyhermüller T, Bill E, Hildebrandt P, Ould-Moussa L, Glaser T, Wieghardt K (mars 1998). "Pourquoi la forme active de la galactose oxydase possède-t-elle un état fondamental diamagnétique?". Angew. Chem. Int. Ed. Engl . 37 (5): 616–619. doi : 10.1002 / (SICI) 1521-3773 (19980316) 37: 5 <616 :: AID-ANIE616> 3.0.CO; 2-4 . PMID 29711069 .
Lectures complémentaires
- Dzik, WI .; Zhang, XP; de Bruin, B. (2011). "Noninnocence Redox des ligands de carbène: Radicaux de carbène dans la formation de liaison CC (catalytique)". Chimie inorganique . 50 (20): 9896–9903. doi : 10.1021 / ic200043a . PMID 21520926 .
- Büttner, T .; Geier, J .; Frison, G .; Harmer, J .; Calle, C .; Schweiger, A .; Schönberg, H .; Grützmacher, H. (2005). "Un Complexe Métallique Radical Aminyl Stable". La science . 307. 307 (5707): 235–238. Bibcode : 2005Sci ... 307..235B . doi : 10.1126 / science.1106070 . PMID 15653498 .
- Hetterscheid, DGH; Kaiser, J .; Reijerse, E .; Peters, TPJ; Thewissen, S .; Blok, ANJ; Smits, JMM; de Gelder, R .; de Bruin, B. (2005). "Ir II (éthène): métal ou carbone radical?". Journal de l'American Chemical Society . 127 (6): 1895-1905. doi : 10.1021 / ja0439470 . PMID 15701024 .
- Blanchard, S.; Derat, E .; Desage-El Murr, M.; Fensterbank, L.; Malacria, M; Mouriès-Mansuy, V. (2012). "Ligands non innocents: nouvelles opportunités dans la catalyse du fer". Journal européen de chimie inorganique . 2012 (3): 376-389. doi : 10.1002 / ejic.201100985 .
- Kaim, W. (2012). "Le monde rétrécissant des ligands innocents: les ligands conventionnels et non conventionnels Redox-Active". Journal européen de chimie inorganique . 2012 (3): 343–348. doi : 10.1002 / ejic.201101359 .