Sélénol - Selenol
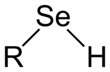
Les sélénols sont des composés organiques qui contiennent le groupe fonctionnel avec la connectivité C– Se –H. Sélénols sont parfois aussi appelés selenomercaptans et selenothiols . Les sélénols sont l'une des principales classes de composés organoséléniés . Le membre le plus connu du groupe est l' acide aminé sélénocystéine .
Structure, collage, propriétés
Les sélénols sont structurellement similaires aux thiols , mais la liaison C-Se est environ 8 % plus longue à 196 pm. L'angle C–Se–H approche 90°. La liaison implique des orbitales p presque pures sur Se, d'où les angles proches de 90. L' énergie de la liaison Se-H est plus faible que la liaison S-H, par conséquent les sélénols sont facilement oxydés et servent de donneurs d'atomes H. La liaison Se-H est beaucoup plus faible que la liaison SH, comme le reflète leur énergie de dissociation de liaison (BDE) respective. Pour C 6 H 5 Se-H, le BDE est de 326 kJ/mol, tandis que pour C 6 H 5 S-H, le BDE est de 368 kJ/mol.
Les acides sélénoliques sont environ 1000 fois plus forts que les thiols : le p K a du CH 3 SeH est de 5,2 contre 8,3 pour le CH 3 SH. La déprotonation fournit l' anion sélénolate , RSe − , dont la plupart des exemples sont hautement nucléophiles et rapidement oxydés par l'air.
Les points d'ébullition des sélénols ont tendance à être légèrement supérieurs à ceux des thiols. Cela peut être attribué à l'importance accrue d'une liaison de van der Waals plus forte pour les atomes plus gros. Les sélénols volatils ont des odeurs très désagréables.
Applications et occurrence
Les sélénols ont peu d'applications commerciales, étant limités par la toxicité élevée du sélénium ainsi que par la sensibilité de la liaison Se-H. Leurs bases conjuguées , les sélénolates, ont des applications limitées en synthèse organique .

Rôle biochimique
Les sélénols sont importants dans certains processus biologiques. Trois enzymes trouvées chez les mammifères contiennent des sélénols sur leurs sites actifs : la glutathion peroxydase , l' iodothyronine déiodinase et la thiorédoxine réductase . Les sélénols contenus dans ces protéines font partie de l' acide aminé essentiel sélénocystéine . Les sélénols fonctionnent comme des agents réducteurs pour donner un dérivé d' acide sélénique (RSe-OH), qui à son tour sont ré-réduits par des enzymes contenant des thiols. Le méthanesélénol (communément appelé « méthylsélénol ») (CH 3 SeH), qui peut être produit in vitro en incubant la sélénométhionine avec une enzyme méthionine gamma-lyase (METase) bactérienne, par méthylation biologique de l'ion séléniure ou in vivo par réduction de l'acide méthaneséléninique ( CH 3 SeO 2 H), a été invoqué pour expliquer l'activité anticancéreuse de certains composés organosélénium. Les précurseurs du méthanesélénol font l'objet de recherches actives dans la prévention et le traitement du cancer. Dans ces études, le méthanesélénol s'avère plus biologiquement actif que l'éthanesélénol ou le 2-propanesélénol.
Préparation
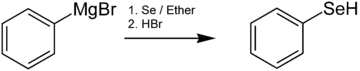
Les sélénols sont généralement préparés par la réaction de réactifs organolithiens ou de réactifs de Grignard avec du Se élémentaire. Par exemple, le benzènesélénol est généré par la réaction du bromure de phénylmagnésium avec le sélénium suivie d'une acidification :
Une autre voie préparatoire aux sélénols implique l' alkylation de la sélénourée , suivie d'une hydrolyse. Les sélénols sont souvent générés par réduction des diséléniures suivie de la protonation du sélénoate résultant :
- 2 RSeSeR + 2 LiHB(C 2 H 5 ) 3 → 2 RSeLi + 2 B(C 2 H 5 ) 3 + H 2
- RSeLi + HCl → RSeH + LiCl
Le diséléniure de diméthyle peut être facilement réduit en méthanesélénol dans les cellules.
Réactions
Les sélénols sont facilement oxydés en diséléniures, composés contenant une liaison Se-Se. Par exemple, le traitement du benzènesélénol avec du brome donne du diphényl diséléniure .
- 2 C 6 H 5 SeH + Br 2 → (C 6 H 5 Se) 2 + 2 HBr
En présence de base, les sélénols sont facilement alkylés pour donner des séléniures. Cette relation est illustrée par la méthylation du méthanesélénol en diméthylséléniure .
Sécurité
Les composés organoséléniés (ou tout composé du sélénium) sont des poisons cumulatifs malgré le fait que des traces de Se sont nécessaires pour la santé.