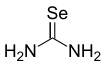
Sélénourée - Selenourea
|
|
|||
| Identifiants | |||
|---|---|---|---|
|
Modèle 3D ( JSmol )
|
|||
| 1734744 | |||
| ChEBI | |||
| ChEMBL | |||
| ChemSpider | |||
| Carte Info ECHA |
100.010.119 |
||
| Numéro CE | |||
| 239756 | |||
| Engrener | C081959 | ||
|
PubChem CID
|
|||
| Numéro RTECS | |||
| UNII | |||
| Numéro UN | 3283 3077 | ||
|
Tableau de bord CompTox ( EPA )
|
|||
|
|||
|
|||
| Propriétés | |||
| CH 4 N 2 Se | |||
| Masse molaire | 123,02 g / mol | ||
| Apparence | Rose / gris uni | ||
| Point de fusion | 200 ° C (392 ° F; 473 K) | ||
| Point d'ébullition | 214 ° C (417 ° F; 487 K) | ||
| Dangers | |||
| Pictogrammes SGH |
  
|
||
| Mot de signalisation SGH | Danger | ||
| H301 , H331 , H373 , H400 , H410 | |||
| P260 , P261 , P264 , P270 , P271 , P273 , P301 + 310 , P304 + 340 , P311 , P314 , P321 , P330 , P391 , P403 + 233 , P405 , P501 | |||
|
Sauf indication contraire, les données sont données pour les matériaux dans leur état standard (à 25 ° C [77 ° F], 100 kPa). |
|||
|
|
|||
| Références Infobox | |||
La sélénourée est le composé organosélénium de formule SeC (NH 2 ) 2 . C'est un solide blanc. Ce composé présente un exemple rare de double liaison carbone-sélénium stable et sans entrave. Le composé est utilisé dans la synthèse d' hétérocycles de sélénium . Par rapport à l' urée , l'analogue oxo de la sélénourée, peu d'études ont été réalisées sur le composé en raison de l'instabilité et de la toxicité des composés du sélénium . La sélénourée est toxique si elle est inhalée ou consommée.
La synthèse
Le composé a été synthétisé pour la première fois en 1884 par Auguste Verneuil par réaction de séléniure d'hydrogène et de cyanamide :
- H 2 Se + NCNH 2 → SeC (NH 2 ) 2
Alors que cette réaction a même trouvé une utilisation dans la synthèse industrielle de sélénourée, des méthodes plus modernes concernent la synthèse de sélénourées substituées. Ceux-ci peuvent être synthétisés à l'aide d'isosélénocyanates organiques et d'amines secondaires:
- RN = C = Se + NHR′R ″ → Se = C (NRH) (NR′R ″ H)
En variante, un carbodiimide substitué pourrait être utilisé comme suit:
- RN = C = NR ′ Se = C (NRH) (NR′H)
Propriétés
Les mesures cristallographiques aux rayons X sur des cristaux à -100 ° C donnent des longueurs moyennes de liaison C = Se de 1,86 Å et de 1,37 Å pour C − N. Les angles Se-C-N et N-C-N ont été mesurés à 120 °, comme prévu pour un carbone hybride sp 2 . Grâce à ces mêmes études, l'existence d' une liaison hydrogène Se-H dans le réseau cristallin - suggérée par la liaison hydrogène O-H et S-H trouvée dans les cristaux d' urée et de thiourée - a été confirmée.
La longueur raccourcie de la liaison N-C et la liaison Se = C plus longue suggèrent une délocalisation de la paire isolée sur les amines; les électrons de liaison Se = C π sont attirés vers l'atome de sélénium, tandis que la paire isolée de l'azote est attirée vers le carbone carbonyle . Un effet similaire est observé dans l'urée et la thiourée. En passant de l'urée à la thiourée en passant par la sélénourée, la double liaison est plus délocalisée et plus longue, tandis que la liaison C − N σ est plus forte et plus courte. En termes de structures de résonance , la forme sélénol (structures II, III) est plus répandue par rapport aux analogues de l'urée et de la thiourée; cependant, le couple isolé l'azote de la sélénourée ne se délocalise que légèrement plus que le couple isolé sur la thiourée (contrairement à une délocalisation beaucoup plus importante en passant de l'urée à la thiourée). Ces différences mineures suggèrent que les propriétés émergeant de la paire isolée d'azote délocalisé et la déstabilisation de la liaison C = S et C = Se π dans la thiourée et la sélénourée seront également similaires.
Contrairement à l'urée et à la thiourée, qui ont toutes deux fait l'objet de recherches approfondies, relativement peu d'études caractérisent quantitativement la sélénourée. Alors que le tautomère de sélone (I) s'est avéré être la forme la plus stable, on dispose principalement d'informations qualitatives et comparatives sur la tautomérisation de la sélénourée .
De manière comparable aux cétones, selones tautomérisent également:
Étant donné que la plus grande délocalisation des électrons de la paire isolée est en corrélation avec le produit de selone, la position d'équilibre de la sélénourée a probablement une position d'équilibre comparable à celle de la thiourée (qui est plus à droite que celle de l'urée). Il a été démontré que la thiourée existe principalement sous sa forme thione à 42 ° C dans du méthanol dilué , le tautomère de thionol étant pratiquement inexistant à pH neutre .
Réactivité
Une classe importante de réactions de sélénourée est la formation d' hétérocycles . Certains hétérocycles contenant du sélénium présentent une activité anti - inflammatoire et antitumorale , entre autres utilisations médicinales. L'utilisation de sélénourée comme précurseur est considérée comme le moyen le plus efficace de synthèse hétérocyclique contenant du sélénium.
Une autre classe de réactions est la complexation de la sélénourée avec des métaux de transition et des métalloïdes . Sa capacité à agir comme un ligand efficace est attribuée à l'effet donneur d'électrons des groupes amino et à la stabilisation consécutive de la liaison π sélénium-métal . Dans les complexes de sélénourée, seule une liaison sélénium-métal a été observée, contrairement aux homologues urée et thiourée, qui se lient également à travers l'atome d'azote.