Réaction de Friedel-Crafts - Friedel–Crafts reaction
| Réaction de Friedel-Crafts | |
|---|---|
| Nommé après |
Artisanat Charles Friedel James |
| Type de réaction | Réaction de couplage |
| Identifiants | |
| ID d'ontologie RSC | RXNO : 0000369 |
Les réactions de Friedel-Crafts sont un ensemble de réactions développées par Charles Friedel et James Crafts en 1877 pour attacher des substituants à un cycle aromatique . Les réactions de Friedel-Crafts sont de deux types principaux : les réactions d' alkylation et les réactions d' acylation . Les deux procèdent par substitution aromatique électrophile .
Alkylation de Friedel-Crafts
| Alkylation de Friedel-Crafts | |
|---|---|
| Nommé après |
Artisanat Charles Friedel James |
| Type de réaction | Réaction de couplage |
| Identifiants | |
| Portail de la chimie organique | friedel-crafts-alkylation |
| ID d'ontologie RSC | RXNO : 0000046 |
Alkylation de Friedel-Crafts comprend l'alkylation d'un cycle aromatique avec un halogénure d'alkyle en utilisant un solide acide de Lewis , tel que le chlorure d'aluminium , le chlorure ferrique , ou un autre MX n réactif, comme catalyseur . Le mécanisme général des halogénures d'alkyle tertiaire est indiqué ci-dessous.
Pour les halogénures d'alkyle primaires (et éventuellement secondaires), un complexe de type carbocation avec l'acide de Lewis, [R (+) ---(X---MX n ) (–) ] est plus susceptible d'être impliqué, plutôt qu'un carbocation gratuite.
Cette réaction présente l'inconvénient que le produit est plus nucléophile que le réactif car les groupes alkyle sont des activateurs de la réaction de Friedel-Crafts . Par conséquent, une suralkylation peut se produire. L'encombrement stérique peut être exploité pour limiter le nombre d'alkylations, comme dans la t- butylation du 1,4-diméthoxybenzène.
De plus, la réaction n'est utile que pour les halogénures d'alkyle primaires dans un sens intramoléculaire lorsqu'un cycle à 5 ou 6 chaînons est formé. Pour le cas intermoléculaire, la réaction est limitée aux agents alkylants tertiaires , à certains agents alkylants secondaires (ceux pour lesquels le réarrangement des carbocations est dégénéré) ou aux agents alkylants qui produisent des carbocations stabilisés (par exemple, benzyliques ou allyliques). Dans le cas des halogénures d'alkyle primaires, le complexe de type carbocation (R (+) ---X---Al (-) Cl 3 ) subira une réaction de réarrangement carbocationique pour donner presque exclusivement le produit réarrangé dérivé d'un carbocation tertiaire.
Alkylations sont pas limités aux halogénures d' alkyle: les réactions de Friedel-Crafts sont possibles avec un carbocationique intermédiaire , tel que ceux dérivés d' alcènes et d' un acide protonique , un acide de Lewis , des énones , et des époxydes . Un exemple est la synthèse de chlorure de néophyle à partir de benzène et de chlorure de méthallyle :
- H 2 C=C(CH 3 )CH 2 Cl + C 6 H 6 → C 6 H 5 C(CH 3 ) 2 CH 2 Cl
Dans une étude, l'électrophile est un ion bromonium dérivé d'un alcène et du NBS :
Dans cette réaction, on pense que le triflate de samarium (III) active le donneur d'halogène NBS dans la formation d'ions halonium.
Désalkylation Friedel-Crafts
L'alkylation de Friedel-Crafts a été supposée réversible . Dans une réaction rétro-Friedel-Crafts ou une désalkylation de Friedel-Crafts , les groupes alkyle sont éliminés en présence de protons ou d'un autre acide de Lewis .
Par exemple, dans une addition multiple de bromure d'éthyle au benzène , une substitution ortho et para est attendue après la première étape de monosubstitution car un groupe alkyle est un groupe activateur . Cependant, le produit de réaction réel est le 1,3,5-triéthylbenzène avec tous les groupes alkyle comme substituant méta . Le contrôle de la réaction thermodynamique garantit que la méta substitution thermodynamiquement favorisée avec un encombrement stérique minimisé prévaut sur la substitution ortho et para moins favorable par équilibrage chimique . Le produit final de la réaction est donc le résultat d'une série d'alkylations et de désalkylations.
Acylation de Friedel-Crafts
| Acylation de Friedel-Crafts | |
|---|---|
| Nommé après |
Artisanat Charles Friedel James |
| Type de réaction | Réaction de couplage |
| Identifiants | |
| Portail de la chimie organique | friedel-crafts-acylation |
| ID d'ontologie RSC | RXNO : 0000045 |
L'acylation de Friedel-Crafts implique l' acylation de cycles aromatiques. Les agents acylants typiques sont les chlorures d'acyle . Les catalyseurs acides de Lewis typiques sont les acides et le trichlorure d'aluminium. Cependant, comme la cétone produite forme un complexe plutôt stable avec les acides de Lewis tels que AlCl 3 , une quantité stoechiométrique ou plus du "catalyseur" doit généralement être utilisée, contrairement au cas de l'alkylation de Friedel-Crafts, dans laquelle le catalyseur est constamment régénéré. L'acylation de Friedel-Crafts est également possible avec les anhydrides d'acide . Les conditions de réaction sont similaires à l'alkylation de Friedel-Crafts. Cette réaction présente plusieurs avantages par rapport à la réaction d'alkylation. En raison de l'effet attracteur d'électrons du groupe carbonyle , le produit cétonique est toujours moins réactif que la molécule d'origine, de sorte que les acylations multiples ne se produisent pas. De plus, il n'y a pas de réarrangements de carbocation , car l' ion acylium est stabilisé par une structure de résonance dans laquelle la charge positive est sur l'oxygène.
La viabilité de l'acylation de Friedel-Crafts dépend de la stabilité du réactif chlorure d'acyle. Le chlorure de formyle, par exemple, est trop instable pour être isolé. Ainsi, la synthèse du benzaldéhyde par la voie Friedel-Crafts nécessite que le chlorure de formyle soit synthétisé in situ . Ceci est accompli par la réaction de Gattermann-Koch , accomplie en traitant le benzène avec du monoxyde de carbone et du chlorure d'hydrogène sous haute pression, catalysée par un mélange de chlorure d'aluminium et de chlorure cuivreux .
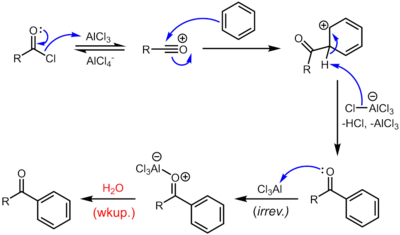
Mécanisme de réaction
La réaction se déroule par génération d'un centre d'acylium. La réaction est complétée par la déprotonation de l' ion arénium par AlCl 4 - , régénérant le catalyseur AlCl 3 . Cependant, contrairement à la réaction d'alkylation véritablement catalytique, la cétone formée est une base de Lewis modérée, qui forme un complexe avec le trichlorure d'aluminium acide fort de Lewis. La formation de ce complexe est typiquement irréversible dans les conditions réactionnelles. Ainsi, une quantité stoechiométrique d'AlCl 3 est nécessaire. Le complexe est détruit lors d'un traitement aqueux pour donner la cétone désirée. Par exemple, la synthèse classique de la désoxybenzoïne fait appel à 1,1 équivalent d'AlCl 3 par rapport au réactif limitant, le chlorure de phénylacétyle. Dans certains cas, généralement lorsque le cycle benzénique est activé, l'acylation de Friedel-Crafts peut également être réalisée avec des quantités catalytiques d'un acide de Lewis plus doux (par exemple des sels de Zn(II)) ou d'un catalyseur acide de Brønsted utilisant l'anhydride ou même l'acide carboxylique lui-même comme agent d'acylation.
Si vous le souhaitez, la cétone résultante peut être ensuite réduite en le substituant alcane correspondant par réduction de Wolff-Kishner ou par réduction de Clemmensen . Le résultat net est le même que l'alkylation de Friedel-Crafts, sauf que le réarrangement n'est pas possible.
hydroxyalkylation de Friedel-Crafts
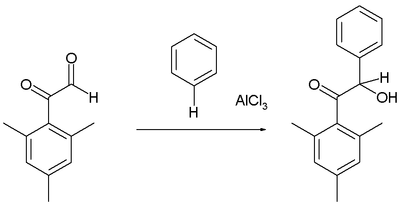
Les arènes réagissent avec certains aldéhydes et cétones pour former les produits hydroxyalkylés, par exemple dans la réaction du dérivé mésitylé du glyoxal avec le benzène :
Comme d'habitude, le groupe aldéhyde est plus électrophile réactif que le phénone .
Portée et variantes
Cette réaction est liée à plusieurs réactions classiques nommées :
- Le produit de réaction acylé peut être converti en produit alkylé via une réduction Clemmensen .
- La réaction de Gattermann-Koch peut être utilisée pour synthétiser le benzaldéhyde à partir du benzène.
- La réaction de Gatterman décrit des réactions d' arène avec de l'acide cyanhydrique.
- La réaction de Houben-Hoesch décrit des réactions arènes avec des nitriles.
- Une modification de la réaction avec un ester phénylique aromatique comme réactif est appelée réarrangement de Fries .
- Dans la réaction de Scholl, deux arènes se couplent directement (parfois appelée arylation de Friedel-Crafts ).
- Dans la réaction de Zincke-Suhl, le p- crésol est alkylé en une cyclohexadiénone avec du tétrachlorométhane.
- Dans la chlorométhylation Blanc, un groupe chlorométhyle est ajouté à un arène avec du formaldéhyde, de l'acide chlorhydrique et du chlorure de zinc.
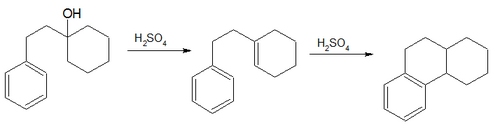
- La synthèse de Bogert-Cook (1933) implique la déshydratation et l' isomérisation du 1-β-phényléthylcyclohexanol en dérivé octahydro du phénanthrène
- La synthèse Darzens-Nenitzescu de cétones (1910, 1936) comprend l'acylation du cyclohexène avec le chlorure d' acétyle à methylcyclohexenylketone.
- Dans l' acylation réductrice de Nenitzescu (1936), un hydrocarbure saturé est ajouté, ce qui en fait une acylation réductrice en méthylcyclohexylcétone
- La réaction de Nencki (1881) est l'acétylation cyclique de phénols avec des acides en présence de chlorure de zinc.
- Dans une variante de la chimie verte, le chlorure d'aluminium est remplacé par du graphite dans une alkylation du p- xylène avec du 2-bromobutane . Cette variation ne fonctionnera pas avec les halogénures primaires à partir desquels moins d'implication de carbocation est déduite.
Colorants
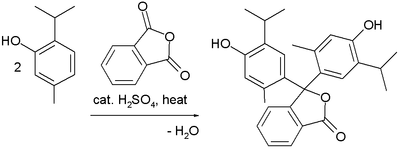
Les réactions de Friedel-Crafts ont été utilisées dans la synthèse de plusieurs colorants triarylméthane et xanthène . Des exemples sont la synthèse de thymolphtaléine (un indicateur de pH) à partir de deux équivalents de thymol et d'anhydride phtalique :
Une réaction de l'anhydride phtalique avec le résorcinol en présence de chlorure de zinc donne le fluorophore fluorescéine . Le remplacement du résorcinol par le N,N-diéthylaminophénol dans cette réaction donne la rhodamine B :
réactions de Haworth
La réaction de Haworth est une méthode classique pour la synthèse de 1-tétralone . Dans cette réaction, le benzène réagit avec l'anhydride succinique , le produit intermédiaire est réduit et une seconde acylation FC a lieu avec addition d'acide.
Dans une réaction apparentée, le phénanthrène est synthétisé à partir de naphtalène et d'anhydride succinique dans une série d'étapes qui commencent par l'acylation FC.
Test Friedel-Crafts pour les hydrocarbures aromatiques
La réaction du chloroforme avec des composés aromatiques à l'aide d'un catalyseur de chlorure d'aluminium donne des triarylméthanes, qui sont souvent de couleur vive, comme c'est le cas dans les colorants triarylméthane. Il s'agit d'un banc d'essai pour les composés aromatiques.
Voir également
- Oxyde d'éthylène
- La famille Friedel , une riche lignée de scientifiques français
- Hydrodéalkylation
- Transalkylation
Les références
- ^ Friedel, C.; Crafts, JM (1877) « Sur une nouvelle méthode générale de synthèse d'hydrocarbures, d'acétones, etc. », Compt. Déchirer. , 84 : 1392 & 1450 .
- ^ Prix, CC (1946). « L'alkylation des composés aromatiques par la méthode Friedel-Crafts ». Org. Réagissez . 3 : 1. doi : 10.1002/0471264180.or003.01 . ISBN 0471264180.
- ^ Bosquets, JK (1972). « L'acylation Friedel-Crafts des alcènes ». Chem. Soc. Rév. 1 : 73. doi : 10.1039/cs9720100073 .
- ^ Eyley, SC (1991). « La réaction aliphatique Friedel-Artisanat ». Comp. Org. Synthé . 2 : 707-731. doi : 10.1016/B978-0-08-052349-1.00045-7 . ISBN 978-0-08-052349-1.
- ^ Heaney, H. (1991). « La réaction aromatique bimoléculaire de Friedel-Artisanat ». Comp. Org. Synthé . 2 : 733–752. doi : 10.1016/B978-0-08-052349-1.00046-9 . ISBN 978-0-08-052349-1.
- ^ Rueping, M.; Nachtsheim, BJ (2010). « Un examen des nouveaux développements dans l'alkylation Friedel-Crafts - De la chimie verte à la catalyse asymétrique » . Beilstein J. Org. Chem . 6 (6) : 6. doi : 10.3762/bjoc.6.6 . PMC 2870981 . PMID 20485588 .
- ^ un b Smith, Michael B.; March, Jerry (2007), Advanced Organic Chemistry: Reactions, Mechanisms, and Structure (6e éd.), New York: Wiley-Interscience, ISBN 978-0-471-72091-1
- ^ L., Williamson, Kenneth (4 janvier 2016). Expériences organiques à l'échelle macro et microscopique . Maîtres, Katherine M. (septième édition). Boston, Massachusetts, États-Unis. ISBN 9781305577190. OCLC 915490547 .
- ^ Smith, WT Jr.; Sellas, JT (1963). "Chlorure de néophyle" . Synthèses organiques .
- ^ Hajra, S.; Maji, B.; Bar, S. (2007). "Samarium Triflate-Catalyzed Halogen-Promoted Friedel-Crafts Alkylation avec des alcènes". Org. Lett. 9 (15) : 2783-2786. doi : 10.1021/ol070813t . PMID 17585769 .
- ^ Anslyn, E.; Wallace, KJ ; Hanes, R.; Morey, J.; Kilway, KV ; Siegel, J. (2005). "Préparation de 1,3,5-Tris(aminométhyl)-2,4,6-triéthylbenzène à partir de deux dérivés polyvalents 1,3,5-Tri(halosubstitué) 2,4,6-triéthylbenzène". Synthèse . 2005 (12) : 2080-2083. doi : 10.1055/s-2005-869963 .
- ^ Norman, Richard Oswald Chandler; Coxon, James Morriss (1993). Principes de synthèse organique (3e éd.). Londres : Blackie Académique & Professionnel. ISBN 0751401269. OCLC 27813843 .
- ^ Somerville, LF; Allen, CFH (1933). "Acide β-benzoylpropionique". Synthèses organiques . 13 : 12. doi : 10.15227/orgsyn.013.0012 .
- ^ "Désoxybenzoïne" . www.orgsyn.org . Récupéré le 26 janvier 2019 .
- ^ Acylation de Friedel-Crafts . Chimie-organique.org. Consulté le 2014-01-11.
- ^ Fuson, RC; Weinstock, HH ; Ullyot, GE (1935). "Une nouvelle synthèse de benjoins. 2′,4′,6′-Trimethylbenzoin". Confiture. Chem. Soc. 57 (10) : 1803-1804. doi : 10.1021/ja01313a015 .
- ^ Clemmensen, E. (1913). "Reduktion von Ketonen und Aldehyden zu den entsprechenden Kohlenwasserstoffen unter Anwendung von amalgamiertem Zink und Salzsäure" . Chemische Berichte . 46 (2) : 1837-1843. doi : 10.1002/cber.19130460292 .
- ^ Clemmensen, E. (1914). "Über eine allgemeine Methode zur Reduktion der Carbonylgruppe in Aldehyden und Ketonen zur Methylengruppe" . Chemische Berichte . 47 : 51-63. doi : 10.1002/cber.19140470108 .
- ^ Clemmensen, E. (1914). "Über eine allgemeine Methode zur Reduktion der Carbonylgruppe in Aldehyden und Ketonen zur Methylengruppe. (III. Mitteilung.)" . Chemische Berichte . 47 : 681-687. doi : 10.1002/cber.191404701107 .
- ^ Gattermann, L.; Koch, JA (1897). "Eine Synthese aromatischer Aldehyde" . Ber. 30 (2) : 1622-1624. doi : 10.1002/cber.18970300288 .
- ^ L. Gattermann; W. Berchelmann (1898). "Synthèse aromatischer Oxyaldéhyde" . Berichte der Deutschen Chemischen Gesellschaft . 31 (2) : 1765-1769. doi : 10.1002/cber.18980310281 .
- ^ Hoesch, Kurt (1915). "Eine neue Synthese aromatischer Ketone. I. Darstellung einiger Phénol-cétone" . Berichte der Deutschen Chemischen Gesellschaft . 48 (1) : 1122-1133. doi : 10.1002/cber.191504801156 .
- ^ Houben, J. (1926). "Über die Kern-Kondensation von Phenolen und Phenol-äthern mit Nitrilen zu Phenol- und Phenol-äther-Ketimiden und -Ketonen (I.)". Berichte der Deutschen Chemischen Gesellschaft (Séries A et B) . 59 (11) : 2878-2891. doi : 10.1002/cber.19260591135 .
- ^ MB Smith, J Mars. Chimie organique avancée de mars (Wiley, 2001) ( ISBN 0-471-58589-0 )
- ^ Grzybowski, M.; Skonieczny, K.; Butenschön, H.; Gryko, DT (2013). « Comparaison du couplage aromatique oxydatif et de la réaction de Scholl ». Angew. Chem. Int. Éd . 52 (38) : 9900-9930. doi : 10.1002/anie.201210238 . PMID 23852649 .
- ^ Zincke, Th. ; Suhl. R. (1906). "Ueber die Einwirkung von Tetrachlorkohlenstoff und Aluminiumchlorid auf p -Kresol und p -Kresolderivate" . Chemische Berichte . 39 (4) : 4148-4153. doi : 10.1002/cber.190603904115 .
-
^ Blanc, Gustave Louis (1923). Bulletin de la Société Chimique de France [4] . 33 : 313-319. Manquant ou vide
|title=( aide ) - ^ G. Grassi et C. Maselli (1898) "Su alcuni derivati clorurati de trossimetilene" (Sur certains dérivés chlorés du 1,3,5-trioxane), Gazzetta Chimica Italiana , 28 (partie 2) : 477-500 ; voir notamment p. 495.
- ^ Cette réaction avec le pentoxyde de phosphore : Kamp, JVD ; Mosettig, E. (1936). "Trans- et Cis-As-Octahydrophénanthrène". Journal de l'American Chemical Society . 58 (6) : 1062-1063. doi : 10.1021/ja01297a514 .
- ^ Nencki, M.; Sieber, N. (1881). "Ueber die Verbindungen der ein- und zweibasischen Fettsäuren mit Phenolen" . J. Prakt. Chem. (en allemand). 23 : 147-156. doi : 10.1002/prac.18810230111 .
- ^ Sereda, Grigoriy A.; Rajpara, Vikul B. (2007). « Une alternative verte à l'alkylation du chlorure d'aluminium du xylène ». J. Chem. Éduc. 2007 (84): 692. bibcode : 2007JChEd..84..692S . doi : 10.1021/ed084p692 .
- ^ McCullagh, James V.; Daggett, Kelly A. (2007). "Synthèse de colorants triarylméthane et xanthène à l'aide de réactions de substitution aromatique électrophile" . J. Chem. Éduc. 84 (11): 1799. bibcode : 2007JChEd..84.1799M . doi : 10.1021/ed084p1799 .
- ^ Haworth, Robert Downs (1932). "Synthèses d'alkylphénanthrènes. Partie I. 1-, 2-, 3- et 4-méthylphénanthrènes". J. Chem. Soc. : 1125. doi : 10.1039/JR9320001125 .
- ^ Li, Jie Jack (2003) Nom des réactions : une collection de mécanismes de réaction détaillés , Springer, ISBN 3-540-40203-9 , p. 175.
- ^ John C. Gilbert., Stephen F. Martin. Brooks/Cole CENGAGE Learning, 2011. pp 872. 25.10 Hydrocarbures aromatiques et halogénures d'aryle - Test de classification. ISBN 978-1-4390-4914-3
Réactions de Friedel-Crafts publiées sur Organic Syntheses
- Alkylations :
- Diphénylacétone, Organic Syntheses, Coll. Vol. 3, p. 343 (1955); Vol. 29, p. 38 (1949) Lien article .
- Réaction du p- xylène avec du chlorométhane en durène Organic Syntheses, Coll. Vol. 2, p. 248 (1943); Vol. 10, p. 32 (1930). Lien de l'article
- Synthèse de la benzophénone à partir du benzène et du tétrachlorométhane Organic Syntheses, Coll. Vol. 1, p. 95 (1941); Vol. 8, p. 26 (1928). Lien de l'article
- Acylations :
- Synthèses organiques de dibenzoyléthylène, Coll. Vol. 3, p. 248 (1955); Vol. 20, p. 29 (1940) Lien article .
- réaction d' acénaphtène plus acide succinique Organic Syntheses, Coll. Vol. 3, p. 6 (1955); Vol. 20, p. 1 (1940). Lien de l'article
- Desoxybenzoin Organic Syntheses, Coll. Vol. 2, p. 156 (1943); Vol. 12, p. 16 (1932). Lien de l'article
- Acylation d'un composé de phénanthrène Organic Syntheses, Vol. 80, p. 227 Lien
- Réaction du bromobenzène avec l'anhydride acétique Organic Syntheses, Coll. Vol. 1, p. 109 (1941); Vol. 5, p. 17 (1925). Lien de l'article
- bêta-méthylanthraquinone, Organic Syntheses, Coll. Vol. 1, p. 353 (1941); Vol. 4, p. 43 (1925). Lien de l'article
- Benzoylation des synthèses organiques du ferrocène , Coll. Vol. 6, p. 625 (1988); Vol. 56, p. 28 (1977). Lien de l'article