Réduction du nitrile - Nitrile reduction
Dans la réduction du nitrile, un nitrile est réduit soit en une amine, soit en un aldéhyde avec un réactif chimique approprié.
Hydrogénation catalytique
L' hydrogénation catalytique des nitriles est souvent la voie la plus économique disponible pour la production d' amines primaires . Les catalyseurs pour la réaction comprennent souvent des métaux du groupe 10 tels que le nickel de Raney , le noir de palladium ou le dioxyde de platine . Cependant, d'autres catalyseurs, tels que le borure de cobalt , peuvent également être sélectifs pour la production d'amine primaire:
- RC≡N + 2 H 2 → R-CH 2 NH 2
Une application commerciale de cette technologie comprend la production d' hexaméthylènediamine à partir d' adiponitrile , un précurseur du Nylon 66 .
En fonction des conditions de réaction , les imines intermédiaires peuvent également subir une attaque par des produits aminés pour donner des amines secondaires et tertiaires :
- 2 RC≡N + 4 H 2 → (R-CH 2 ) 2 NH + NH 3
- 3 RC≡N + 6 H 2 → (R-CH 2 ) 3 N + 2 NH 3
De telles réactions se déroulent via des intermédiaires d' énamine . La condition de réaction la plus importante pour la production sélective d'amine primaire est le choix du catalyseur. D'autres facteurs importants incluent le choix du solvant , le pH de la solution , les effets stériques , la température et la pression de l'hydrogène.
Réductions stoechiométriques
Les agents réducteurs pour la conversion non catalytique en amines comprennent l'hydrure de lithium et d'aluminium , le borohydrure de lithium , le diborane ou le sodium élémentaire dans des solvants alcooliques .
Aux aldéhydes
Les nitriles peuvent également être réduits en aldéhydes . La synthèse d'aldéhyde de Stephen utilise du chlorure d'étain (II) et de l'acide chlorhydrique pour produire un aldéhyde via l' hydrolyse d'un sel d' iminium résultant . Des aldéhydes peuvent également se former en utilisant un donneur d'hydrogène suivi d'une hydrolyse in situ d'une imine. Des réactifs utiles pour cette réaction comprennent l'acide formique avec une catalyse d'hydrogénation ou des hydrures métalliques qui sont utilisés pour ajouter une mole d'hydrogène au nitrile. Par exemple, le borohydrure de sodium réduit les nitriles dans les solvants alcooliques avec un catalyseur CoCl 2 ou du nickel de Raney . Agent réducteur L'hydrure de diisobutylaluminium , ou DIBAL-H, est un autre hydrure métallique couramment utilisé. Le DIBAL-H agit comme une source d'hydrure, ajoutant un ion hydrure au carbone du nitrile. L'imine résultante est un intermédiaire relativement stable qui peut être hydrolysé en aldéhyde.
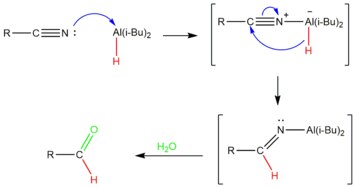
Mécanisme
Le DIBAL-H est ajouté en quantités contrôlées à basse température pour obtenir une réduction partielle du nitrile. L'atome d'aluminium dans DIBAL agit comme un acide de Lewis , acceptant une paire d'électrons du nitrile. Le nitrile est ensuite réduit par le transfert d'un ion hydrure sur le carbone de la triple liaison carbone-nitrile, produisant une imine. Après un traitement avec de l'eau, le complexe d'aluminium est hydrolysé pour produire l'aldéhyde souhaité. Parce que le traitement hydrolytique génère l'aldéhyde à la fin, le nitrile ne subit pas de sur-réduction.
Méthodes électrochimiques
Les nitriles de benzyle peuvent également être réduits par voie électrochimique .