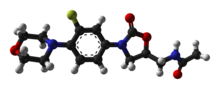
Linézolide - Linezolid
 | |
 | |
| Donnée clinique | |
|---|---|
| Prononciation | / L ɪ n ɛ z əl ɪ d , - n eɪ z - / |
| Appellations commerciales | Zyvox, Zyvoxid, autres |
| AHFS / Drugs.com | Monographie |
| MedlinePlus | a602004 |
| Données de licence | |
Catégorie grossesse |
|
| Voies d' administration |
Infusion intraveineuse , par voie orale |
| Classe de médicament | Antibiotique oxazolidinone |
| code ATC | |
| Statut légal | |
| Statut légal | |
| Données pharmacocinétiques | |
| Biodisponibilité | ~100% (orale) |
| Liaison protéique | Faible (31%) |
| Métabolisme | foie (50-70%, CYP non impliqué) |
| Demi-vie d' élimination | 3 à 7 heures ; demi-vie plus longue dans le LCR que le plasma |
| Excrétion | non rénal, rénal et fécal |
| Identifiants | |
| |
| Numero CAS | |
| CID PubChem | |
| Banque de médicaments | |
| ChemSpider | |
| UNII | |
| KEGG | |
| ChEBI | |
| ChEMBL | |
| NIAID ChemDB | |
| Ligand PDB | |
| Tableau de bord CompTox ( EPA ) | |
| Carte d'information de l'ECHA |
100.121.520 |
| Données chimiques et physiques | |
| Formule | C 16 H 20 F N 3 O 4 |
| Masse molaire | 337,351 g·mol -1 |
| Modèle 3D ( JSmol ) | |
| |
| |
| (Vérifier) | |
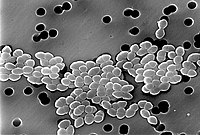
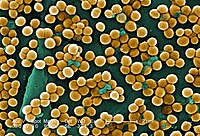
Linézolide est un antibiotique utilisé pour le traitement des infections causées par des bactéries Gram-positives qui sont résistantes à d' autres antibiotiques. Le linézolide est actif contre la plupart des bactéries à Gram positif qui causent la maladie, y compris les streptocoques , les entérocoques résistants à la vancomycine (ERV) et Staphylococcus aureus résistant à la méthicilline (SARM). Les principales utilisations sont les infections de la peau et la pneumonie, bien qu'il puisse être utilisé pour une variété d'autres infections, y compris la tuberculose résistante aux médicaments . Il est utilisé soit par injection dans une veine, soit par voie orale.
Lorsqu'il est administré pendant de courtes périodes, le linézolide est un antibiotique relativement sûr. Il peut être utilisé chez les personnes de tous âges et chez les personnes atteintes d' une maladie du foie ou d'une mauvaise fonction rénale . Les effets secondaires courants avec une utilisation à court terme comprennent les maux de tête , la diarrhée , les éruptions cutanées et les nausées . Les effets secondaires graves peuvent inclure le syndrome sérotoninergique , la suppression de la moelle osseuse et des taux élevés de lactate dans le sang , en particulier lorsqu'il est utilisé pendant plus de deux semaines. S'il est utilisé pendant de longues périodes, il peut provoquer des lésions nerveuses , y compris des lésions du nerf optique , qui peuvent être irréversibles.
En tant qu'inhibiteur de la synthèse des protéines , le linézolide agit en supprimant la production de protéines bactériennes . Cela arrête la croissance ou entraîne la mort bactérienne . Bien que de nombreux antibiotiques fonctionnent de cette façon, le mécanisme d'action exact du linézolide semble être unique en ce qu'il bloque l'initiation de la production de protéines, plutôt que l'une des étapes ultérieures. En 2014, la résistance bactérienne au linézolide est restée faible. Le linézolide fait partie de la classe des médicaments oxazolidinone .
Le linézolide a été découvert au milieu des années 1990 et son utilisation commerciale a été approuvée en 2000. Il figure sur la liste des médicaments essentiels de l'Organisation mondiale de la santé . L'Organisation mondiale de la santé classe le linézolide comme étant d'une importance critique pour la médecine humaine. Le linézolide est disponible sous forme de médicament générique .
Utilisations médicales
La principale utilisation du linézolide est le traitement des infections graves causées par aérobie bactéries Gram-positives qui sont résistants à d' autres antibiotiques; il ne doit pas être utilisé contre les bactéries sensibles aux médicaments à spectre d'activité plus étroit, tels que les pénicillines et les céphalosporines . Dans la presse populaire et la littérature scientifique, le linézolide a été qualifié d'« antibiotique de réserve », à utiliser avec parcimonie afin de rester efficace comme médicament de dernier recours contre les infections potentiellement incurables.
Aux États-Unis, les indications d'utilisation du linézolide approuvées par la Food and Drug Administration (FDA) des États-Unis sont le traitement des infections à Enterococcus faecium résistantes à la vancomycine , avec ou sans invasion bactérienne de la circulation sanguine ; pneumonie nosocomiale (acquise à l'hôpital) et pneumonie communautaire causée par S. aureus ou S. pneumoniae ; infections compliquées de la peau et des structures cutanées (cSSSI) causées par des bactéries sensibles, y compris une infection du pied diabétique , à moins qu'elle ne soit compliquée par une ostéomyélite (infection des os et de la moelle osseuse); et les infections de la peau et des tissus mous non compliquées causées par S. pyogenes ou S. aureus . Le fabricant déconseille l'utilisation du linézolide pour la pneumonie communautaire ou les infections de la peau et des tissus mous non compliquées causées par le SARM. Au Royaume-Uni, la pneumonie et les cSSSI sont les seules indications notées sur l'étiquetage du produit.
Le linézolide semble être aussi sûr et efficace chez les enfants et les nouveau-nés que chez les adultes.
Infections de la peau et des tissus mous
Une grande méta-analyse d'essais contrôlés randomisés a révélé que le linézolide était plus efficace que les antibiotiques glycopeptidiques (tels que la vancomycine et la teicoplanine ) et les antibiotiques bêta-lactamines dans le traitement des infections de la peau et des tissus mous (ITSS) causées par des bactéries à Gram positif, et des études plus petites semblent confirmer sa supériorité sur la teicoplanine dans le traitement de toutes les infections graves à Gram positif.
Dans le traitement des infections du pied diabétique, le linézolide semble être moins cher et plus efficace que la vancomycine. Dans une étude ouverte de 2004 , il était aussi efficace que l' ampicilline/sulbactam et l' amoxicilline/acide clavulanique , et bien supérieur chez les patients présentant des ulcères du pied et sans ostéomyélite , mais avec des taux d'effets indésirables significativement plus élevés. Cependant, une méta-analyse de 18 essais contrôlés randomisés en 2008 a révélé que le traitement au linézolide échouait aussi souvent que les autres antibiotiques, que les patients souffraient ou non d'ostéomyélite.
Certains auteurs ont recommandé d'essayer des combinaisons de médicaments moins chers ou plus rentables (tels que le cotrimoxazole avec la rifampicine ou la clindamycine ) avant le linézolide dans le traitement des SSTI lorsque la sensibilité de l'organisme en cause le permet.
Pneumonie
Aucune différence significative n'apparaît dans les taux de réussite du traitement entre le linézolide, les glycopeptides ou les antibiotiques bêta-lactamines appropriés dans le traitement de la pneumonie. Les directives cliniques pour le traitement de la pneumonie communautaire développées par l' American Thoracic Society et l' Infectious Diseases Society of America recommandent que le linézolide soit réservé aux cas dans lesquels le SARM a été confirmé comme l'organisme causal, ou lorsqu'une infection à SARM est suspectée sur la base de la présentation clinique. Les directives de la British Thoracic Society ne le recommandent pas comme traitement de première intention, mais plutôt comme alternative à la vancomycine. Le linézolide est également un traitement de deuxième intention acceptable pour la pneumonie à pneumocoques d'origine communautaire en cas de résistance à la pénicilline.
Les directives américaines recommandent le linézolide ou la vancomycine comme traitement de première intention de la pneumonie à SARM nosocomiale nosocomiale. Certaines études ont suggéré que le linézolide est meilleur que la vancomycine contre la pneumonie nosocomiale, en particulier la pneumonie associée au ventilateur causée par le SARM, peut-être parce que la pénétration du linézolide dans les fluides bronchiques est beaucoup plus élevée que celle de la vancomycine. Cependant, plusieurs problèmes dans la conception de l'étude ont été soulevés, remettant en cause les résultats qui suggèrent la supériorité du linézolide. Quoi qu'il en soit, les avantages du linézolide incluent sa biodisponibilité orale élevée - qui permet de passer facilement à un traitement oral - et le fait qu'une mauvaise fonction rénale n'est pas un obstacle à son utilisation. En revanche, il est très difficile d' obtenir le dosage correct de vancomycine chez les patients souffrant d' insuffisance rénale .
Autre
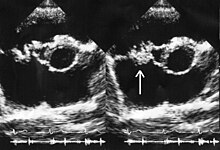
Il est traditionnellement admis que les infections dites « profondes », telles que l'ostéomyélite ou l'endocardite infectieuse, doivent être traitées avec des antibiotiques bactéricides et non bactériostatiques. Néanmoins, des études précliniques ont été menées pour évaluer l'efficacité du linézolide pour ces infections, et le médicament a été utilisé avec succès pour les traiter en pratique clinique. Le linézolide semble être une option thérapeutique raisonnable pour l'endocardite infectieuse causée par des bactéries Gram-positives multirésistantes, malgré le manque de preuves de haute qualité pour étayer cette utilisation. Les résultats dans le traitement de l'endocardite entérococcique ont varié, certains cas étant traités avec succès et d'autres ne répondant pas au traitement. Des preuves de qualité faible à moyenne s'accumulent également pour son utilisation dans les infections des os et des articulations, y compris l'ostéomyélite chronique, bien que les effets indésirables soient une préoccupation importante lorsqu'une utilisation à long terme est nécessaire.
En association avec d'autres médicaments, le linézolide a été utilisé pour traiter la tuberculose . La dose optimale à cet effet n'a pas été établie. Chez l'adulte, des doses quotidiennes et biquotidiennes ont été utilisées à bon escient. De nombreux mois de traitement sont souvent nécessaires et le taux d'effets indésirables est élevé quel que soit le dosage. Il n'y a pas suffisamment de preuves fiables d'efficacité et d'innocuité pour étayer cette indication en tant qu'utilisation de routine.
Le linézolide a été étudié comme alternative à la vancomycine dans le traitement de la neutropénie fébrile chez les patients cancéreux lorsqu'une infection à Gram positif est suspectée. C'est également l'un des rares antibiotiques qui diffusent dans l' humeur vitrée et peut donc être efficace dans le traitement de l' endophtalmie (inflammation des parois internes et des cavités de l'œil) causée par des bactéries sensibles. Encore une fois, il existe peu de preuves de son utilisation dans ce contexte, car l'endophtalmie infectieuse est traitée largement et efficacement avec de la vancomycine injectée directement dans l'œil .
Infections du système nerveux central
Dans les études animales sur la méningite causée par Streptococcus pneumoniae , le linézolide s'est avéré bien pénétrer dans le liquide céphalo-rachidien , mais son efficacité était inférieure à celle d'autres antibiotiques. Il ne semble pas y avoir suffisamment de preuves de haute qualité pour soutenir l'utilisation systématique du linézolide pour traiter la méningite bactérienne. Néanmoins, il a été utilisé avec succès dans de nombreux cas d' infection du système nerveux central , y compris la méningite, causée par des bactéries sensibles, et a également été suggéré comme un choix raisonnable pour cette indication lorsque les options de traitement sont limitées ou lorsque d'autres antibiotiques ont échoué. Les directives de l'Infectious Diseases Society of America recommandent le linézolide comme médicament de choix de première intention pour la méningite à ERV et comme alternative à la vancomycine pour la méningite à SARM. Le linézolide semble supérieur à la vancomycine dans le traitement des infections communautaires à SARM du système nerveux central, bien que très peu de cas de telles infections aient été publiés (en 2009).
En mars 2007, la FDA a publié les résultats d' un essai clinique de phase III randomisé , ouvert , comparant le linézolide à la vancomycine dans le traitement des infections sanguines liées aux cathéters . Les patients traités par la vancomycine pourraient passer à l' oxacilline ou à la dicloxacilline si la bactérie à l'origine de leur infection s'avérait sensible, et les patients des deux groupes (linézolide et vancomycine) pourraient recevoir un traitement spécifique contre les bactéries à Gram négatif si nécessaire. L'étude elle-même a été publiée en janvier 2009.
Le linézolide a été associé à une mortalité significativement plus élevée que les antibiotiques de comparaison. Lorsque les données de tous les participants ont été regroupées, l'étude a révélé que 21,5% de ceux qui avaient reçu du linézolide sont décédés, contre 16% de ceux qui n'en ont pas reçu. La différence s'est avérée être due à l'infériorité du linézolide dans le traitement des infections à Gram négatif seules ou mixtes à Gram négatif/Gram positif. Chez les participants dont l'infection était due à des bactéries Gram-positives seules, le linézolide était aussi sûr et efficace que la vancomycine. À la lumière de ces résultats, la FDA a émis une alerte rappelant aux professionnels de la santé que le linézolide n'est pas approuvé pour le traitement des infections liées aux cathéters ou des infections causées par des organismes à Gram négatif, et qu'un traitement plus approprié doit être instauré chaque fois qu'une infection à Gram négatif est confirmé ou suspecté.
Populations spécifiques
Chez les adultes et les enfants de plus de 12 ans, le linézolide est généralement administré toutes les 12 heures, que ce soit par voie orale ou intraveineuse. Chez les jeunes enfants et les nourrissons, il est administré toutes les huit heures. Aucun ajustement posologique n'est nécessaire chez les personnes âgées, chez les personnes atteintes d'insuffisance hépatique légère à modérée ou chez celles dont la fonction rénale est altérée. Chez les personnes nécessitant une hémodialyse , il faut veiller à administrer du linézolide après une séance, car la dialyse enlève 30 à 40 % d'une dose de l'organisme ; aucun ajustement posologique n'est nécessaire chez les personnes subissant une hémofiltration continue , bien qu'une administration plus fréquente puisse être justifiée dans certains cas. Selon une étude, le linézolide peut devoir être administré plus fréquemment que la normale chez les personnes souffrant de brûlures affectant plus de 20 % de la surface corporelle , en raison de l'augmentation de la clairance non rénale du médicament.
Le linézolide appartient à la catégorie de grossesse C aux États-Unis , ce qui signifie qu'il n'y a pas eu d'études adéquates sur son innocuité lorsqu'il est utilisé par des femmes enceintes, et bien que des études animales aient montré une légère toxicité pour le fœtus, les avantages de l'utilisation du médicament peuvent l'emporter sur ses risques. Il passe également dans le lait maternel , bien que la signification clinique de ceci (le cas échéant) soit inconnue.
Spectre d'activité
Le linézolide est efficace contre les bactéries Gram-positives cliniquement importantes bactéries -ceux dont la paroi cellulaire contient une épaisse couche de peptidoglycane et aucune membrane externe -notamment Enterococcus faecium et Enterococcus de (y compris la vancomycine entérocoques résistants ), Staphylococcus aureus (résistant à la méthicilline , y compris Staphylococcus aureus , MRSA), Streptococcus agalactiae , Streptococcus pneumoniae , Streptococcus pyogenes , les streptocoques du groupe viridans , Listeria monocytogenes , et les espèces de Corynebacterium (cette dernière étant parmi les plus sensibles au linézolide, avec des concentrations minimales inhibitrices systématiquement inférieures à 0,5 mg/L). Le linézolide est également très actif in vitro contre plusieurs mycobactéries . Il semble être très efficace contre Nocardia , mais en raison de son coût élevé et de ses effets indésirables potentiellement graves, les auteurs ont recommandé qu'il soit associé à d'autres antibiotiques ou réservé aux cas ayant échoué au traitement traditionnel.
Le linézolide est considéré comme bactériostatique contre la plupart des organismes, c'est-à-dire qu'il arrête leur croissance et leur reproduction sans les tuer réellement, mais a une certaine activité bactéricide (tueuse) contre les streptocoques. Certains auteurs ont noté que, malgré son effet bactériostatique in vitro , le linézolide « se comporte » comme un antibiotique bactéricide in vivo car il inhibe la production de toxines par les staphylocoques et les streptocoques. Il a également un effet post-antibiotique d'une durée d'une à quatre heures pour la plupart des bactéries, ce qui signifie que la croissance bactérienne est temporairement supprimée même après l'arrêt du médicament.
Bactéries à Gram négatif
Le linézolide n'a pas d'effet cliniquement significatif sur la plupart des bactéries à Gram négatif . Les Pseudomonas et les Enterobacteriaceae , par exemple, ne sont pas sensibles. In vitro , il est actif contre Pasteurella multocida , Fusobacterium , Moraxella catarrhalis , Legionella , Bordetella et Elizabethkingia meningoseptica , et modérément actif (ayant une concentration minimale inhibitrice pour 90 % des souches de 8 mg/L) contre Haemophilus influenzae . Il a également été utilisé à bon escient comme traitement de deuxième intention pour les infections à Capnocytophaga .
Antibiotiques comparables
Le spectre d'activité du linézolide contre les bactéries Gram-positives est similaire à celui de l' antibiotique glycopeptidique vancomycine , qui a longtemps été la norme pour le traitement des infections à SARM, et les deux médicaments sont souvent comparés. D'autres antibiotiques comparables comprennent des antibiotiques glycopeptidiques tels que la teicoplanine (nom commercial Targocid), la dalbavancine (Dalvance) et la télavancine (Vibativ); quinupristine/dalfopristine (Synercid, une combinaison de deux streptogramines , non active contre E. faecalis ) ; la daptomycine (Cubicin, un lipopeptide ); et le ceftobiprole (Zevtera, une céphalosporine de 5e génération ). Le linézolide est le seul qui peut être pris par voie orale pour le traitement des infections systémiques. À l'avenir, l' oritavancine et l' iclaprim pourraient être des alternatives orales utiles au linézolide – les deux en sont aux premiers stades de développement clinique.
Effets indésirables
Lorsqu'il est utilisé pendant de courtes périodes, le linézolide est un médicament relativement sûr. Les effets secondaires courants de l'utilisation du linézolide (ceux qui surviennent chez plus de 1 % des personnes prenant du linézolide) comprennent la diarrhée (signalée par 3 à 11 % des participants aux essais cliniques), les maux de tête (1 à 11 %), les nausées (3 à 10 %), vomissements (1 à 4 %), éruption cutanée (2 %), constipation (2 %), altération de la perception du goût (1 à 2 %) et décoloration de la langue (0,2 à 1 %). Des infections fongiques telles que le muguet et la candidose vaginale peuvent également survenir car le linézolide supprime la flore bactérienne normale et ouvre une niche pour les champignons (appelée candidose antibiotique ). Les effets indésirables moins fréquents (et potentiellement plus graves) incluent des réactions allergiques, une pancréatite et des transaminases élevées , qui peuvent être un signe de lésions hépatiques. Contrairement à certains antibiotiques, tels que l' érythromycine et les quinolones , le linézolide n'a aucun effet sur l' intervalle QT , une mesure de la conduction électrique cardiaque . Les effets indésirables chez les enfants sont similaires à ceux qui surviennent chez les adultes.
Comme presque tous les antibiotiques, le linézolide a été associé à la diarrhée associée à Clostridium difficile ( DACD ) et à la colite pseudomembraneuse , bien que cette dernière soit rare, survenant chez environ un patient sur deux mille dans les essais cliniques. C. difficile semble être sensible au linézolide in vitro , et le linézolide a même été considéré comme un traitement possible de la DACD.
Utilisation à long terme
Une aplasie médullaire , caractérisée notamment par une thrombocytopénie (faible numération plaquettaire), peut survenir au cours du traitement par le linézolide ; il semble que ce soit le seul effet indésirable qui se produit significativement plus fréquemment avec le linézolide qu'avec les glycopeptides ou les bêta-lactamines. Elle est rare chez les patients qui reçoivent le médicament pendant 14 jours ou moins, mais survient beaucoup plus fréquemment chez les patients qui reçoivent des cures plus longues ou qui souffrent d'insuffisance rénale. Un rapport de cas de 2004 a suggéré que la pyridoxine (une forme de vitamine B 6 ) pouvait inverser l'anémie et la thrombocytopénie causées par le linézolide, mais une étude ultérieure plus importante n'a trouvé aucun effet protecteur.
L'utilisation à long terme du linézolide a également été associée à une neuropathie périphérique induite par la chimiothérapie , un engourdissement par des picotements progressif et persistant souvent irréversible, une douleur intense et une hypersensibilité au froid, commençant dans les mains et les pieds et impliquant parfois les bras et les jambes. Les médicaments de chimiothérapie associés à CIPN comprennent thalidomide , les épothilones tels que ixabépilone , le vinca alcaloïdes vincristine et vinblastine , le taxanes paclitaxel et docétaxel , les inhibiteurs de protéasome tels que bortezomib , et les médicaments à base de platine cisplatine , oxaliplatine et carboplatine . et la neuropathie optique , qui est plus fréquente après plusieurs mois de traitement et peut également être irréversible. Bien que le mécanisme de lésion soit encore mal compris, la toxicité mitochondriale a été proposée comme cause ; le linézolide est toxique pour les mitochondries , probablement en raison de la similitude entre les ribosomes mitochondriaux et bactériens . L'acidose lactique , une accumulation potentiellement mortelle d' acide lactique dans le corps, peut également survenir en raison d'une toxicité mitochondriale. En raison de ces effets à long terme, le fabricant recommande des numérations globulaires complètes hebdomadaires pendant le traitement par le linézolide pour surveiller une éventuelle suppression de la moelle osseuse, et recommande que le traitement ne dure pas plus de 28 jours. Un protocole de surveillance plus étendu pour la détection précoce de la toxicité chez les patients gravement malades recevant du linézolide a été développé et proposé par une équipe de chercheurs à Melbourne, en Australie. Le protocole comprend des tests sanguins bihebdomadaires et des tests de la fonction hépatique ; mesure des taux sériques de lactate , pour la détection précoce de l'acidose lactique ; un examen de tous les médicaments pris par le patient, interrompant l'utilisation de ceux qui peuvent interagir avec le linézolide ; et des examens oculaires et neurologiques périodiques chez les patients devant recevoir du linézolide pendant plus de quatre semaines.
Les effets indésirables du traitement à long terme par le linézolide ont été identifiés pour la première fois lors de la surveillance post-commercialisation. La suppression de la moelle osseuse n'a pas été identifiée au cours des essais de phase III, dans lesquels le traitement n'a pas dépassé 21 jours. Bien que certains participants des premiers essais aient présenté une thrombocytopénie, celle-ci s'est avérée réversible et ne s'est pas produite significativement plus fréquemment que chez les témoins (participants ne prenant pas de linézolide). Il y a également eu des rapports post-commercialisation de convulsions et, en 2009, un seul cas de paralysie de Bell (paralysie du nerf facial ) et de toxicité rénale . Des preuves de l'inhibition de la synthèse des protéines dans les cellules de mammifères par le linézolide ont été publiées.
Interactions
Le linézolide est un inhibiteur faible, non sélectif et réversible de la monoamine oxydase (IMAO) et ne doit pas être utilisé en même temps que d'autres IMAO, de grandes quantités d' aliments riches en tyramine (comme le porc, les fromages vieillis, les boissons alcoolisées ou les aliments fumés et marinés). ), ou des médicaments sérotoninergiques . Des cas de syndrome sérotoninergique ont été signalés après la commercialisation lorsque le linézolide a été administré avec ou peu après l'arrêt des médicaments sérotoninergiques, en particulier des inhibiteurs sélectifs de la recapture de la sérotonine tels que la paroxétine et la sertraline . Il peut également augmenter les effets d'augmentation de la pression artérielle des médicaments sympathomimétiques tels que la pseudoéphédrine ou la phénylpropanolamine . Il ne doit pas non plus être administré en association avec la péthidine ( mépéridine ) en aucune circonstance en raison du risque de syndrome sérotoninergique .
Le linézolide n'inhibe ni n'induit le système du cytochrome P450 (CYP), qui est responsable du métabolisme de nombreux médicaments couramment utilisés, et n'a donc pas d'interactions liées au CYP.
Pharmacologie
Pharmacodynamique
Le linézolide, comme les autres oxazolidinones, est un inhibiteur de la synthèse des protéines bactériennes et un inhibiteur faible, non sélectif et réversible de la monoamine oxydase . En tant qu'inhibiteur de la synthèse des protéines, le linézolide arrête la croissance et la reproduction des bactéries en perturbant la traduction de l'ARN messager (ARNm) en protéines dans les ribosomes bactériens . Le linézolide inhibe la traduction lors de la première étape de la synthèse protéique, l' initiation , contrairement à la plupart des autres inhibiteurs de la synthèse protéique, qui inhibent l' élongation . Il le fait en empêchant la formation du complexe d'initiation, composé des sous - unités 30S et 50S du ribosome, de l' ARNt et de l'ARNm. Le linézolide se lie à la partie 23S de la sous-unité 50S (le centre de l' activité de la peptidyl transférase ), à proximité des sites de liaison du chloramphénicol , de la lincomycine et d'autres antibiotiques. En raison de ce mécanisme d'action unique, la résistance croisée entre le linézolide et d'autres inhibiteurs de la synthèse des protéines est très peu fréquente ou inexistante.
En 2008, la structure cristalline du linézolide lié à la sous-unité 50S d'un ribosome de l' archéen Haloarcula marismortui a été élucidée par une équipe de scientifiques de l'Université de Yale et déposée dans la Protein Data Bank . Une autre équipe a déterminé en 2008 la structure du linézolide lié à une sous-unité 50S de Deinococcus radiodurans . Les auteurs ont proposé un modèle affiné pour le mécanisme d'action des oxazolidinones, constatant que le linézolide occupe le site A de la sous-unité ribosomique 50S, induisant un changement de conformation qui empêche l'ARNt d'entrer dans le site et force finalement l'ARNt à se séparer du ribosome.
Pharmacocinétique
L'un des avantages du linézolide est qu'il a une biodisponibilité orale absolue de 100 % en raison de son absorption rapide et complète après administration orale ; en d'autres termes, la totalité de la dose atteint la circulation sanguine, comme si elle avait été administrée par voie intraveineuse . Cela signifie que les personnes recevant du linézolide par voie intraveineuse peuvent passer au linézolide par voie orale dès que leur état le permet, alors que des antibiotiques comparables (tels que la vancomycine et la quinupristine/dalfopristine) ne peuvent être administrés que par voie intraveineuse. La prise de linézolide avec de la nourriture ralentit quelque peu son absorption, mais la zone sous la courbe n'est pas affectée.
La liaison aux protéines plasmatiques du linézolide est d'environ 31 % (intervalle de 4 à 32 % ) et son volume de distribution à l' état d'équilibre est en moyenne de 36,1 à 47,3 litres chez des volontaires adultes en bonne santé. Les concentrations plasmatiques maximales (C max ) sont atteintes une à deux heures après l'administration du médicament. Le linézolide est facilement distribué dans tous les tissus du corps, à l'exception de la matrice osseuse et du tissu adipeux blanc . Notamment, la concentration de linézolide dans le liquide de revêtement épithélial (ELF) des voies respiratoires inférieures est au moins égale et souvent supérieure à celle obtenue dans le sérum (certains auteurs ont rapporté des concentrations dans le liquide bronchique jusqu'à quatre fois supérieures aux concentrations sériques). ), ce qui peut expliquer son efficacité dans le traitement de la pneumonie. Cependant, une méta-analyse d'essais cliniques a révélé que le linézolide n'était pas supérieur à la vancomycine , qui atteint des concentrations plus faibles dans l'ELF. Les concentrations de liquide céphalo-rachidien (LCR) varient; les concentrations maximales dans le LCR sont inférieures à celles du sérum, en raison de la diffusion lente à travers la barrière hémato-encéphalique , et les concentrations minimales dans le LCR sont plus élevées pour la même raison. La demi-vie moyenne est de trois heures chez les enfants, de quatre heures chez les adolescents et de cinq heures chez les adultes.
Le linézolide est métabolisé dans le foie , par oxydation du cycle morpholine , sans implication du système du cytochrome P450 . Cette voie métabolique conduit à deux métabolites inactifs majeurs (qui représentent chacun environ 45 % et 10 % d'une dose excrétée à l'état d'équilibre), un métabolite mineur et plusieurs métabolites traces, dont aucun ne représente plus de 1 % d'une dose excrétée. dose. La clairance du linézolide varie avec l'âge et le sexe; elle est la plus rapide chez les enfants (ce qui explique la demi-vie plus courte) et semble être 20 % plus faible chez les femmes que chez les hommes. Il existe une forte corrélation entre la clairance du linézolide et la clairance de la créatinine.
Chimie
Au pH physiologique (7,4), le linézolide existe à l'état non chargé. Il est modérément soluble dans l'eau (environ 3 mg/mL), avec un log P de 0,55.
![Formule schématique du N-{[(5S)-3-[3-fluoro-4-(morpholin-4-yl)phényl]-2-oxo-1,3-oxazolidin-5-yl]méthyl}acétamide, mettant en évidence le les groupes morpholino et fluoro en orange, le reste en bleu. Les atomes de carbone de la chaîne mère sont numérotés.](https://upload.wikimedia.org/wikipedia/commons/thumb/e/ea/Linezolid_showing_oxazolidinone_pharmacophore.svg/220px-Linezolid_showing_oxazolidinone_pharmacophore.svg.png)
L'oxazolidinone pharmacophore -la essentiel « template » chimique pour antimicrobiennes activité -consists d'un 1,3-oxazolidin-2-one fragment avec un groupe aryle groupe en position 3 et un S - groupe méthyle , avec un autre substituant attaché à lui, à la position 5 (les énantiomères R - de toutes les oxazolidinones sont dépourvus de propriétés antibiotiques). En plus de ce noyau essentiel, le linézolide contient également plusieurs caractéristiques structurelles qui améliorent son efficacité et sa sécurité. Un substituant acétamide sur le groupe 5-méthyle est le meilleur choix en termes d'efficacité antibactérienne, et est utilisé dans toutes les oxazolidinones les plus actives développées jusqu'à présent ; en fait, s'éloigner trop d'un groupe acétamide à cette position fait perdre au médicament son pouvoir antimicrobien, bien qu'une activité faible à modérée soit maintenue lorsque certains groupes isostériques sont utilisés. Un atome de fluor en position 3' double pratiquement l'activité in vitro et in vivo , et l' atome d' azote donneur d' électrons dans le cycle morpholine aide à maintenir une puissance antibiotique élevée et un profil d'innocuité acceptable.
L' anticoagulant rivaroxaban (Xarelto) présente une ressemblance structurelle frappante avec le linézolide ; les deux médicaments partagent le pharmacophore de l'oxazolidinone, ne différant que dans trois domaines (une cétone supplémentaire et du chlorothiophène , et il manque l'atome de fluor). Cependant, cette similitude semble n'avoir aucune signification clinique.
Synthèse
Le linézolide est un médicament entièrement synthétique : il n'est pas présent dans la nature (contrairement à l'érythromycine et à de nombreux autres antibiotiques) et n'a pas été développé en s'appuyant sur un squelette naturel (contrairement à la plupart des bêta-lactamines , qui sont semi - synthétiques ). De nombreuses approches sont disponibles pour la synthèse de l'oxazolidinone, et plusieurs voies pour la synthèse du linézolide ont été rapportées dans la littérature chimique. Malgré de bons rendements , la méthode originale (développée par Upjohn pour la production à l'échelle d'une usine pilote de linézolide et d'épérezolid) est longue, nécessite l'utilisation de produits chimiques coûteux, tels que le palladium sur charbon et les réactifs très sensibles chlorure de méthanesulfonyle et n- butyllithium, et a besoin de conditions de basse température. Une grande partie du coût élevé du linézolide a été attribuée au coût de sa synthèse. Un itinéraire un peu plus concis et rentable mieux adapté à la production à grande échelle a été breveté par Upjohn en 1998.
Des synthèses ultérieures ont inclus une méthode « économiquement atomique » à partir de D- mannitol , développée par la société pharmaceutique indienne Dr. Reddy's et rapportée en 1999, et une voie à partir de ( S )-glycéraldéhyde acétonide (préparé à partir d'acide ascorbique ), développée par une équipe de chercheurs de l'Université normale du Hunan à Changsha , Hunan , Chine. Le 25 Juin 2008, au cours de la 12e conférence annuelle de la chimie verte et du génie à New York, Pfizer a rapporté le développement de leur synthèse de linézolide « deuxième génération »: un convergent , vert synthèse à partir de ( S ) - épichlorhydrine , avec un rendement supérieur et une réduction de 56 % des déchets totaux.
La résistance
Une résistance acquise au linézolide a été signalée dès 1999, chez deux patients atteints d'une infection grave et multirésistante à Enterococcus faecium qui ont reçu le médicament dans le cadre d'un programme d' usage compassionnel . Staphylococcus aureus résistant au linézolide a été isolé pour la première fois en 2001.
Aux États-Unis, la résistance au linézolide est surveillée et suivie depuis 2004 par le biais d'un programme nommé LEADER, qui (en 2007) a été mené dans 60 établissements médicaux à travers le pays. La résistance est restée stable et extrêmement faible — moins d'un demi pour cent des isolats dans l' ensemble et moins d'un dixième de un pour cent des échantillons de S. aureus . Un programme mondial similaire, la « Zyvox Annual Appraisal of Potency and Spectrum Study », ou ZAAPS, est mené depuis 2002. En 2007, la résistance globale au linézolide dans 23 pays était inférieure à 0,2 % et inexistante chez les streptocoques. La résistance n'a été trouvée qu'au Brésil, en Chine, en Irlande et en Italie, parmi les staphylocoques à coagulase négative (0,28 % des échantillons résistants), les entérocoques (0,11 %) et S. aureus (0,03 %). Au Royaume-Uni et en Irlande, aucune résistance n'a été trouvée chez les staphylocoques prélevés sur des cas de bactériémie entre 2001 et 2006, bien qu'une résistance chez les entérocoques ait été signalée. Certains auteurs ont prédit que la résistance d' E. faecium augmentera si l'utilisation du linézolide se poursuit aux niveaux actuels ou augmente. Néanmoins, le linézolide continue d'être un agent antimicrobien important avec une activité presque complète (résistance à 0,05 %).
Mécanisme
La résistance intrinsèque de la plupart des bactéries Gram-négatives au linézolide est due à l'activité des pompes d'efflux , qui « pompent » activement le linézolide hors de la cellule plus rapidement qu'il ne peut s'accumuler.
Les bactéries à Gram positif développent généralement une résistance au linézolide à la suite d'une mutation ponctuelle connue sous le nom de G2576T , dans laquelle une base guanine est remplacée par la thymine dans la paire de bases 2576 des gènes codant pour l'ARN ribosomique 23S. C'est le mécanisme de résistance le plus courant chez les staphylocoques, et le seul connu à ce jour chez les isolats d' E . faecium . D'autres mécanismes ont été identifiés chez Streptococcus pneumoniae (notamment des mutations dans une ARN méthyltransférase qui méthyle G2445 de l'ARNr 23S et des mutations provoquant une expression accrue des gènes transporteurs ABC ) et chez Staphylococcus epidermidis .
Histoire
Les oxazolidinones sont connues comme inhibiteurs de la monoamine oxydase depuis la fin des années 1950. Leurs propriétés antimicrobiennes ont été découvertes par des chercheurs de l' IE du Pont de Nemours dans les années 1970. En 1978, DuPont a breveté une série de dérivés d'oxazolidinone comme étant efficaces dans le traitement des maladies bactériennes et fongiques des plantes , et en 1984, un autre brevet a décrit leur utilité dans le traitement des infections bactériennes chez les mammifères . En 1987, les scientifiques de DuPont ont présenté une description détaillée des oxazolidinones en tant que nouvelle classe d'antibiotiques avec un nouveau mécanisme d'action . Cependant, les premiers composés ont produit une toxicité hépatique et le développement a été interrompu.
Pharmacia & Upjohn (qui fait maintenant partie de Pfizer) a lancé son propre programme de recherche sur l'oxazolidinone dans les années 1990. Les études des relations structure-activité des composés ont conduit au développement de plusieurs sous-classes de dérivés d'oxazolidinone, avec des profils d'innocuité et une activité antimicrobienne variables. Deux composés ont été considérés comme des candidats médicaments : l' épérezolid (nom de code PNU-100592 ) et le linézolide ( PNU-100766 ). Aux stades précliniques de développement, ils étaient similaires en termes de sécurité et d'activité antibactérienne, ils ont donc été soumis à des essais cliniques de phase I pour identifier toute différence de pharmacocinétique . Le linézolide s'est avéré avoir un avantage pharmacocinétique - ne nécessitant qu'une dose deux fois par jour, tandis que l'épérezolid devait être administré trois fois par jour pour obtenir une exposition similaire - et a donc procédé à d'autres essais. La Food and Drug Administration (FDA) des États-Unis a approuvé le linézolide le 18 avril 2000. L'approbation a suivi au Brésil (juin 2000), au Royaume-Uni (janvier 2001), au Japon et au Canada (avril 2001), en Europe (tout au long de 2001) et dans d'autres pays en Amérique latine et en Asie.
En 2009, le linézolide était le seul antibiotique oxazolidinone disponible. D'autres membres de cette classe sont entrés en développement, tels que le posizolid (AZD2563), le ranbézolide (RBx 7644) et le radezolid (RX-1741). En 2014, la FDA a approuvé le phosphate de tédizolide , un dérivé d'oxazolidinone de deuxième génération, pour les infections bactériennes aiguës de la peau et des structures cutanées.
Société et culture
Économie
Le linézolide était assez cher en 2009 ; un traitement peut coûter un ou deux mille dollars américains pour le médicament seul, sans parler des autres coûts (comme ceux associés au séjour à l'hôpital). Le médicament devenant générique, le prix a baissé. En Inde, en 2015, un mois de linézolide, tel qu'il serait utilisé pour traiter la tuberculose, coûtait environ 60 $ US.
Cependant, étant donné que le linézolide intraveineux peut être remplacé par une formulation orale (comprimés ou solution buvable) sans compromettre l'efficacité, les personnes peuvent quitter l'hôpital relativement tôt et poursuivre le traitement à domicile, alors que le traitement à domicile avec des antibiotiques injectables peut être peu pratique. La réduction de la durée d'hospitalisation réduit le coût global du traitement, même si le linézolide peut avoir un coût d'acquisition plus élevé, c'est-à-dire qu'il peut être plus cher, que des antibiotiques comparables.
Des études ont été menées dans plusieurs pays avec différents modèles de système de santé pour évaluer la rentabilité du linézolide par rapport aux glycopeptides tels que la vancomycine ou la teicoplanine. Dans la plupart des pays, le linézolide était plus rentable que des antibiotiques comparables pour le traitement de la pneumonie nosocomiale et des infections compliquées de la peau et des structures cutanées, soit en raison de taux de guérison et de survie plus élevés, soit en raison des coûts de traitement globaux inférieurs.
En 2009, Pfizer a payé 2,3 milliards de dollars et a conclu un accord d'intégrité d'entreprise pour régler les accusations selon lesquelles elle avait mal étiqueté et fait la promotion illégale de quatre médicaments, et fait en sorte que de fausses déclarations soient soumises aux programmes de santé gouvernementaux pour des utilisations qui n'avaient pas été approuvées par l'United States Food and Administration des médicaments. 1,3 milliard de dollars ont été payés pour régler des accusations criminelles de commercialisation illégale de l'anti-inflammatoire valdécoxib , tandis qu'un milliard de dollars a été payé en amendes civiles pour commercialisation illégale de trois autres médicaments, dont le Zyvox.
Les noms de marques
| UNE | Amizole 500 (Kenya), Anozilad (Pologne), Antizolid (Grèce), Arlid (Inde), Arlin (Bangladesh), Averozolid & Debacozoline (Egypte) |
| B | |
| C | |
| ré | Dilizolen (Pologne, Slovaquie, Pays-Bas, Bulgarie) |
| E | Entavar (Inde) |
| F | |
| g | Grampolid (Pays-Bas), Grampolyve (Pays-Bas), Gramposimide (Pologne, Pays-Bas), Grampoxid (Pays-Bas) |
| H | |
| je | |
| J | |
| K | |
| L | Lidobact (Pays-Bas), Linez (Bangladesh, Égypte), Linezolid Accord (Pays-Bas), Linezolid Amneal (Pays-Bas), Linezolid Betapharm (Pays-Bas), Linezolid Farmaprojects (Pays-Bas), Linezolid Fresenius Kabi (Pays-Bas), Linezolid GNP (Égypte), Linezolid Hetero (Pays-Bas), Linezolid Kabi (Croatie, Pologne), Linezolid Mylan (Pays-Bas), Linezolid Pfizer (Pays-Bas), Linezolid Pliva (Croatie), Linezolid Polpharma (Pays-Bas, Pologne), Linezolid Richet (Argentine), Linezolid Sandoz (Belgique, Suisse, Pays-Bas, Slovaquie, Estonie, Croatie, Pologne), Linezolid Teva (Pays-Bas, Roumanie), Linezolid Zentiva (Pologne), Linezolida Teva (Portugal), Linezone (Turquie), Linid (Inde), Linosept (Inde), Linozid ( Bangladesh), Linxyd (Pays-Bas), Linzolid (Bangladesh), Linzowin (Inde), Litrecan (Argentine), Livegramide (Pays-Bas), Lizbid (Inde), Lizemox (Inde), Lizolid (Inde, Vietnam), Lizoliden (Pays-Bas), Lizomac (Inde), Lizomed (Inde), Lizorex (Inde), Lizox (Pays-Bas) lands), Lorezogram (Pays-Bas), Lynvox (Pays-Bas), Lynz (Croatie) |
| M | |
| N | Natlinez (Pays-Bas) |
| O | |
| P | Pneumolid (Croatie, Pays-Bas, Pologne, Roumanie, Bulgarie) |
| Q | |
| R | Ralinz (Inde), Respenzo (Egypte) |
| S | Synzolid (Pays-Bas) |
| T | |
| U | |
| V | Voxazoldine (Égypte) |
| W | |
| X | |
| Oui | |
| Z | Zenix (Bosnie-Herzégovine, Serbie), Zizolid (Turquie), Zodlin (Inde), Zolinid (Bulgarie), Zyvox (Géorgie, Chili, Argentine, Australie, Chine, Équateur, Égypte, Royaume-Uni, Hong Kong, Indonésie, Irlande, Corée du Sud, Malte, Malaisie, Nouvelle-Zélande, Philippines, Singapour, Thaïlande, Taïwan, Japon, États-Unis), Zyvoxam (Canada), Zyvoxid (Israël, Autriche, Belgique, Bulgarie, Suisse, République tchèque, Danemark, Estonie, Espagne, Finlande, France, Grèce, Allemagne, Croatie, Islande, Lituanie, Lettonie, Pays-Bas, Norvège, Portugal, Roumanie, Suède, Slovaquie, Tunisie, Turquie, Afrique du Sud, Pologne, Italie, Bosnie-Herzégovine) |
| Combinaison générique | Marque |
|---|---|
| linézolide et céfixime | Zifi-Turbo (Inde) |
Les références
Liens externes
- "Linézolide" . Portail d'information sur les médicaments . Bibliothèque nationale de médecine des États-Unis.