Métabolisme des acides gras - Fatty acid metabolism
Le métabolisme des acides gras consiste en divers processus métaboliques impliquant ou étroitement liés aux acides gras , une famille de molécules classées dans la catégorie des macronutriments lipidiques . Ces processus peuvent principalement être divisés en (1) processus cataboliques qui génèrent de l'énergie et (2) processus anaboliques où ils servent de blocs de construction pour d'autres composés.
Dans le catabolisme, les acides gras sont métabolisés pour produire de l'énergie, principalement sous forme d' adénosine triphosphate (ATP). Comparés à d'autres classes de macronutriments (glucides et protéines), les acides gras produisent le plus d'ATP sur une base énergétique par gramme, lorsqu'ils sont complètement oxydés en CO 2 et en eau par la bêta-oxydation et le cycle de l'acide citrique . Les acides gras (principalement sous forme de triglycérides ) sont donc la principale forme de stockage de carburant chez la plupart des animaux, et dans une moindre mesure chez les végétaux.
Dans l'anabolisme, les acides gras intacts sont des précurseurs importants des triglycérides, des phospholipides, des seconds messagers, des hormones et des corps cétoniques . Par exemple, les phospholipides forment les bicouches phospholipidiques à partir desquelles toutes les membranes de la cellule sont construites à partir d'acides gras. Les phospholipides comprennent la membrane plasmique et d'autres membranes qui renferment tous les organites des cellules, tels que le noyau , les mitochondries , le réticulum endoplasmique et l'appareil de Golgi . Dans un autre type d'anabolisme, les acides gras sont modifiés pour former une myriade d'autres composés. Par exemple, certains seconds messagers et hormones locales . Les prostaglandines fabriquées à partir d' acide arachidonique stocké dans la membrane cellulaire, sont probablement le groupe le plus connu de ces hormones locales.
Catabolisme des acides gras
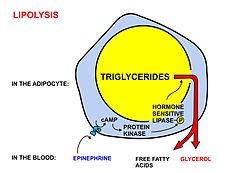


Les acides gras sont stockés sous forme de triglycérides dans les dépôts graisseux du tissu adipeux . Entre les repas, ils sont libérés comme suit :
- La lipolyse , l'élimination des chaînes d'acides gras du glycérol auquel elles sont liées sous leur forme de stockage sous forme de triglycérides (ou graisses), est réalisée par des lipases . Ces lipases sont activées par des taux élevés d' épinéphrine et de glucagon dans le sang (ou de noradrénaline sécrétée par les nerfs sympathiques dans le tissu adipeux), provoqués par la baisse de la glycémie après les repas, ce qui abaisse simultanément le taux d' insuline dans le sang.
- Une fois débarrassés du glycérol , les acides gras libres pénètrent dans le sang, qui les transporte, attachés à l' albumine plasmatique , dans tout l'organisme.
- Les acides gras libres à longue chaîne pénètrent dans les cellules métabolisantes (c'est-à-dire la plupart des cellules vivantes du corps, à l'exception des globules rouges et des neurones du système nerveux central ) via des protéines de transport spécifiques , telles que la protéine de transport des acides gras de la famille SLC27 . Les globules rouges ne contiennent pas de mitochondries et sont donc incapables de métaboliser les acides gras ; les tissus du système nerveux central ne peuvent pas utiliser d'acides gras, bien qu'ils contiennent des mitochondries, car les acides gras à longue chaîne (par opposition aux acides gras à chaîne moyenne) ne peuvent pas traverser la barrière hémato-encéphalique dans les liquides interstitiels qui baignent ces cellules.
- Une fois à l'intérieur de la cellule, l' acide gras à longue chaîne-CoA ligase catalyse la réaction entre une molécule d'acide gras avec l' ATP (qui est décomposé en AMP et en pyrophosphate inorganique) pour donner un acyl-adénylate gras, qui réagit ensuite avec la coenzyme A libre pour donner une molécule d' acyl-CoA gras .
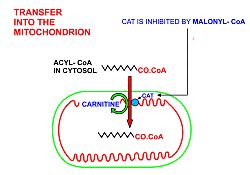
- Pour que l'acyl-CoA pénètre dans la mitochondrie, la navette carnitine est utilisée :
- L'acyl-CoA est transféré au groupe hydroxyle de la carnitine par la carnitine palmitoyltransférase I , située sur les faces cytosoliques des membranes mitochondriales externe et interne .
- L'acyl-carnitine est transportée à l'intérieur par une translocase carnitine-acylcarnitine , comme une carnitine est transportée à l'extérieur.
- L'acyl-carnitine est reconvertie en acyl-CoA par la carnitine palmitoyltransférase II , située sur la face interne de la membrane mitochondriale interne . La carnitine libérée est renvoyée vers le cytosol, comme un acyl-CoA est transporté dans la matrice mitochondriale.
- La bêta-oxydation , dans la matrice mitochondriale, coupe ensuite les longues chaînes carbonées des acides gras (sous forme de molécules d'acyl-CoA) en une série d' unités à deux carbones ( acétate ) qui, combinées à la co-enzyme A , forment molécules d' acétyl CoA , qui se condensent avec l' oxaloacétate pour former du citrate au « début » du cycle de l'acide citrique . Il est commode de considérer cette réaction comme marquant le "point de départ" du cycle, car c'est à ce moment-là que le carburant - l'acétyl-CoA - est ajouté au cycle, qui sera dissipé sous forme de CO 2 et H 2 O avec la libération de une quantité substantielle d'énergie captée sous forme d' ATP , au cours de chaque tour du cycle.
- En bref, les étapes de la bêta-oxydation (la décomposition initiale des acides gras libres en acétyl-CoA) sont les suivantes :
- Déshydrogénation par acyl-CoA déshydrogénase , donnant 1 FADH 2
- Hydratation par l' énoyl-CoA hydratase
- Déshydrogénation par 3-hydroxyacyl-CoA déshydrogénase , donnant 1 NADH + H +
- Clivage par la thiolase , donnant 1 acétyl-CoA et un acide gras qui a maintenant été raccourci de 2 carbones (formant un nouvel acyl-CoA raccourci )
- Cette réaction d'oxydation bêta est répétée jusqu'à ce que l'acide gras soit complètement réduit en acétyl-CoA ou, dans le cas des acides gras à nombre impair d'atomes de carbone, en acétyl-CoA et 1 molécule de propionyl-CoA par molécule d'acide gras. Chaque coupe bêta oxydative de la molécule d'acyl-CoA produit 5 molécules d' ATP .
- L'acétyl-CoA produit par oxydation bêta entre dans le cycle de l'acide citrique dans la mitochondrie en se combinant avec l' oxaloacétate pour former le citrate . Il en résulte la combustion complète de l'acétyl-CoA en CO 2 et en eau. L'énergie libérée dans ce processus est captée sous forme de 1 GTP et 11 molécules d' ATP par molécule d'acétyl-CoA oxydée. C'est le sort de l'acétyl-CoA partout où la bêta-oxydation des acides gras se produit, sauf dans certaines circonstances dans le foie .
Dans le foie, l'oxaloacétate peut être totalement ou partiellement détourné vers la voie gluconéogène pendant le jeûne, la famine, un régime pauvre en glucides, un exercice intense prolongé et dans le diabète sucré de type 1 non contrôlé . Dans ces circonstances, l'oxaloacétate est hydrogéné en malate qui est ensuite éliminé des mitochondries des cellules hépatiques pour être converti en glucose dans le cytoplasme des cellules hépatiques, d'où il est libéré dans le sang. Dans le foie, par conséquent, l'oxaloacétate n'est pas disponible pour la condensation avec l'acétyl-CoA lorsque la néoglucogenèse significative a été stimulée par une insuline faible (ou absente) et des concentrations élevées de glucagon dans le sang. Dans ces circonstances, l'acétyl-CoA est détourné vers la formation d' acétoacétate et de bêta-hydroxybutyrate . L'acétoacétate, le bêta-hydroxybutyrate et leur produit de dégradation spontanée, l' acétone , sont fréquemment, mais de manière confuse, connus sous le nom de corps cétoniques (car ce ne sont pas du tout des "corps", mais des substances chimiques solubles dans l'eau). Les cétones sont libérées par le foie dans le sang. Toutes les cellules avec des mitochondries peuvent extraire les cétones du sang et les reconvertir en acétyl-CoA, qui peut ensuite être utilisé comme carburant dans leurs cycles d'acide citrique, car aucun autre tissu ne peut détourner son oxaloacétate dans la voie gluconéogène de la manière dont cela peut se produire dans le foie. Contrairement aux acides gras libres, les cétones peuvent traverser la barrière hémato-encéphalique et sont donc disponibles comme carburant pour les cellules du système nerveux central , agissant comme un substitut du glucose, sur lequel ces cellules survivent normalement. L'apparition de taux élevés de cétones dans le sang pendant la famine, un régime pauvre en glucides, un exercice intense prolongé et un diabète sucré de type 1 non contrôlé est connue sous le nom de cétose et, dans sa forme extrême, de diabète sucré de type 1 incontrôlé , que l' acidocétose .
- Le glycérol libéré par l'action de la lipase est phosphorylé par la glycérol kinase dans le foie (le seul tissu dans lequel cette réaction peut se produire), et le glycérol 3-phosphate résultant est oxydé en dihydroxyacétone phosphate . L'enzyme glycolytique triose phosphate isomérase convertit ce composé en glycéraldéhyde 3-phosphate , qui est oxydé via la glycolyse , ou converti en glucose via la néoglucogenèse .
Les acides gras comme source d'énergie

Les acides gras, stockés sous forme de triglycérides dans un organisme, sont une importante source d'énergie car ils sont à la fois réduits et anhydres . Le rendement énergétique d'un gramme d'acides gras est d'environ 9 kcal (37 kJ), contre 4 kcal (17 kJ) pour les glucides. Étant donné que la partie hydrocarbure des acides gras est hydrophobe , ces molécules peuvent être stockées dans un environnement relativement anhydre (sans eau). Les glucides, en revanche, sont plus hydratés. Par exemple, 1 g de glycogène peut lier environ 2 g d' eau , ce qui se traduit par 1,33 kcal/g (4 kcal/3 g). Cela signifie que les acides gras peuvent contenir plus de six fois la quantité d'énergie par unité de masse de stockage. En d'autres termes, si le corps humain comptait sur les glucides pour stocker de l'énergie, une personne aurait besoin de transporter 31 kg (67,5 lb ) de glycogène hydraté pour avoir l'énergie équivalente à 4,6 kg (10 lb) de graisse .
Les animaux en hibernation sont un bon exemple d'utilisation des réserves de graisse comme combustible. Par exemple, les ours hibernent pendant environ 7 mois et, pendant toute cette période, l'énergie provient de la dégradation des réserves de graisse. Les oiseaux migrateurs accumulent également d'importantes réserves de graisse avant de se lancer dans leurs voyages intercontinentaux.
Ainsi, les réserves de graisse du jeune adulte humain se situent en moyenne entre 10 et 20 kg, mais varient considérablement en fonction de l'âge, du sexe et de la disposition individuelle. En revanche, le corps humain ne stocke qu'environ 400 g de glycogène , dont 300 g sont bloqués à l'intérieur des muscles squelettiques et ne sont pas disponibles pour le corps dans son ensemble. Les 100 g environ de glycogène stockés dans le foie sont épuisés dans la journée qui suit la famine. Par la suite, le glucose qui est libéré dans le sang par le foie pour une utilisation générale par les tissus du corps, doit être synthétisé à partir des acides aminés glucogéniques et de quelques autres substrats gluconéogènes , qui ne comprennent pas les acides gras. A noter cependant que la lipolyse libère du glycérol qui peut entrer dans la voie de la néoglucogenèse.
Synthèse des glucides à partir du glycérol et des acides gras
Les acides gras sont décomposés en acétyl-CoA par oxydation bêta à l'intérieur des mitochondries, tandis que les acides gras sont synthétisés à partir d'acétyl-CoA à l'extérieur des mitochondries, dans le cytosol. Les deux voies sont distinctes, non seulement dans l'endroit où elles se produisent, mais aussi dans les réactions qui se produisent et les substrats qui sont utilisés. Les deux voies sont mutuellement inhibitrices, empêchant l'acétyl-CoA produit par bêta-oxydation d'entrer dans la voie de synthèse via la réaction acétyl-CoA carboxylase . Il ne peut pas non plus être converti en pyruvate car la réaction du complexe pyruvate déshydrogénase est irréversible. Au lieu de cela, l'acétyl-CoA produit par la bêta-oxydation des acides gras se condense avec l' oxaloacétate , pour entrer dans le cycle de l'acide citrique . À chaque tour du cycle, deux atomes de carbone quittent le cycle sous forme de CO 2 dans les réactions de décarboxylation catalysées par l' isocitrate déshydrogénase et l' alpha-cétoglutarate déshydrogénase . Ainsi, chaque tour du cycle de l'acide citrique oxyde une unité acétyl-CoA tout en régénérant la molécule d'oxaloacétate avec laquelle l'acétyl-CoA s'était initialement combiné pour former l'acide citrique . Les réactions de décarboxylation se produisent avant la formation du malate dans le cycle. Seules les plantes possèdent les enzymes pour convertir l'acétyl-CoA en oxaloacétate à partir duquel le malate peut être formé pour être finalement converti en glucose.
Cependant, l'acétyl-CoA peut être converti en acétoacétate, qui peut se décarboxyler en acétone (soit spontanément, soit par l' acétoacétate décarboxylase ). Il peut ensuite être métabolisé en isopropanol qui est excrété dans l'haleine/l'urine, ou par le CYP2E1 en hydroxyacétone (acétol). L'acétol peut être converti en propylène glycol . Celui-ci se transforme en formiate et en acétate (ce dernier se convertissant en glucose), ou en pyruvate (par deux enzymes alternatives), ou en propionaldéhyde , ou en L- lactaldéhyde puis L- lactate (l'isomère lactate commun). Une autre voie transforme l'acétol en méthylglyoxal , puis en pyruvate , ou en D -lactaldéhyde (via SD -lactoyl-glutathion ou autre) puis en D -lactate . Le métabolisme du D-lactate (en glucose) est lent ou altéré chez l'homme, de sorte que la majeure partie du D-lactate est excrétée dans l'urine; ainsi, le D- lactate dérivé de l'acétone peut contribuer de manière significative à l'acidose métabolique associée à la cétose ou à l'intoxication à l'isopropanol. Le L- lactate peut compléter la conversion nette des acides gras en glucose. La première expérience à montrer la conversion de l'acétone en glucose a été réalisée en 1951. Ceci, et d'autres expériences ont utilisé le marquage isotopique du carbone . Jusqu'à 11% du glucose peut être dérivé de l'acétone pendant la famine chez les humains.
Le glycérol libéré dans le sang lors de la lipolyse des triglycérides dans le tissu adipeux ne peut être absorbé que par le foie. Il est ici transformé en glycérol 3-phosphate par action de la glycérol kinase qui hydrolyse une molécule d' ATP par molécule de glycérol phosphorylée. Le glycérol 3-phosphate est ensuite oxydé en dihydroxyacétone phosphate , qui est à son tour converti en glycéraldéhyde 3-phosphate par l'enzyme triose phosphate isomérase . De là , les trois atomes de carbone du glycérol d' origine peuvent être oxydés via la glycolyse , ou convertis en glucose via la néoglucogenèse .
Autres fonctions et utilisations des acides gras
Signalisation intracellulaire
Les acides gras font partie intégrante des phospholipides qui constituent la majeure partie des membranes plasmiques , ou membranes cellulaires, des cellules. Ces phospholipides peuvent être clivés en diacylglycérol (DAG) et l' inositol triphosphate (IP 3 ) par hydrolyse du phospholipide, le phosphatidylinositol 4,5-bisphosphate (PIP 2 ), par la membrane cellulaire lié enzyme phospholipase C (PLC).
Hormones eicosanoïdes paracrines
Un produit du métabolisme des acides gras sont les prostaglandines , des composés ayant divers effets hormonaux chez les animaux. Les prostaglandines ont été trouvées dans presque tous les tissus humains et autres animaux. Ils sont dérivés enzymatiquement de l'acide arachidonique, un acide gras polyinsaturé à 20 carbones. Chaque prostaglandine contient donc 20 atomes de carbone, dont un cycle à 5 carbones . Ils sont une sous-classe des eicosanoïdes et forment la classe des prostanoïdes des dérivés d'acides gras.
Les prostaglandines sont synthétisées dans la membrane cellulaire par clivage de l'arachidonate des phospholipides qui composent la membrane. Celle-ci est catalysée soit par la phospholipase A 2 agissant directement sur un phospholipide membranaire, soit par une lipase agissant sur le DAG (diacyl-glycérol). L'arachidonate est ensuite sollicité par le composant cyclooxygénase de la prostaglandine synthase . Cela forme un cycle cyclopentane à peu près au milieu de la chaîne d'acides gras. La réaction ajoute également 4 atomes d'oxygène dérivés de deux molécules d'O 2 . La molécule résultante est la prostaglandine G 2 qui est converti par le composant hydroperoxydase du complexe d'enzyme dans la prostaglandine H 2 . Ce composé très instable se transforme rapidement en d'autres prostaglandines, prostacycline et thromboxanes. Ceux-ci sont ensuite libérés dans les fluides interstitiels entourant les cellules qui ont fabriqué l'hormone eicosanoïde.
Si l'arachidonate est sollicité par une lipoxygénase au lieu de la cyclooxygénase, des acides hydroxyéicosatétraénoïques et des leucotriènes sont formés. Ils agissent également comme des hormones locales.
Les prostaglandines ont deux dérivés : les prostacyclines et les thromboxanes . Les prostacyclines sont de puissants vasodilatateurs à action locale et inhibent l'agrégation des plaquettes sanguines . Par leur rôle dans la vasodilatation, les prostacyclines sont également impliquées dans l' inflammation . Ils sont synthétisés dans les parois des vaisseaux sanguins et remplissent la fonction physiologique de prévenir la formation inutile de caillots, ainsi que de réguler la contraction du tissu musculaire lisse . A l'inverse, les thromboxanes (produits par les cellules plaquettaires) sont des vasoconstricteurs et facilitent l'agrégation plaquettaire. Leur nom vient de leur rôle dans la formation du caillot ( thrombose ).
Sources alimentaires d'acides gras, leur digestion, leur absorption, leur transport dans le sang et leur stockage

Une proportion importante des acides gras de l'organisme provient de l'alimentation, sous forme de triglycérides d'origine animale ou végétale. Les acides gras contenus dans les graisses provenant d'animaux terrestres ont tendance à être saturés, tandis que les acides gras contenus dans les triglycérides des poissons et des plantes sont souvent polyinsaturés et donc présents sous forme d'huiles.
Ces triglycérides , ne peuvent pas être absorbés par l' intestin . Ils sont décomposés en mono- et di-glycérides plus acides gras libres (mais pas de glycérol libre) par la lipase pancréatique , qui forme un complexe 1:1 avec une protéine appelée colipase (également un constituant du suc pancréatique), qui est nécessaire pour son activité. Le complexe activé ne peut agir qu'à l'interface eau-graisse. Par conséquent, il est essentiel que les graisses soient d'abord émulsionnées par les sels biliaires pour une activité optimale de ces enzymes. Les produits de digestion constitués d'un mélange de tri-, di- et monoglycérides et d'acides gras libres qui, avec les autres contenus liposolubles de l'alimentation (par exemple les vitamines liposolubles et le cholestérol) et les sels biliaires forment des micelles mixtes , dans le contenu duodénal aqueux (voir schémas à droite).
Le contenu de ces micelles (mais pas les sels biliaires) pénètre dans les entérocytes (cellules épithéliales tapissant l'intestin grêle) où ils sont resynthétisés en triglycérides et conditionnés en chylomicrons qui sont libérés dans les lactés (les capillaires du système lymphatique des intestins ). Ces lactés s'écoulent dans le canal thoracique qui se jette dans le sang veineux à la jonction des veines jugulaire gauche et sous-clavière gauche sur le côté inférieur gauche du cou. Cela signifie que les produits liposolubles de la digestion sont rejetés directement dans la circulation générale, sans passer d'abord par le foie, comme le font tous les autres produits de digestion. La raison de cette particularité est inconnue.
Les chylomicrons circulent dans tout le corps, donnant au plasma sanguin un aspect laiteux ou crémeux après un repas gras. La lipoprotéine lipase sur les surfaces endothéliales des capillaires, en particulier dans le tissu adipeux , mais dans une moindre mesure également dans d'autres tissus, digère partiellement les chylomicrons en acides gras libres, en glycérol et en restes de chylomicrons. Les acides gras sont absorbés par les adipocytes, mais les restes de glycérol et de chylomicrons restent dans le plasma sanguin, pour être finalement éliminés de la circulation par le foie. Les acides gras libres libérés par la digestion des chylomicrons sont absorbés par les adipocytes, où ils sont resynthétisés en triglycérides à l'aide de glycérol dérivé du glucose dans la voie glycolytique . Ces triglycérides sont stockés, jusqu'à ce qu'ils soient nécessaires pour les besoins en carburant des autres tissus, dans la goutte de graisse de l' adipocyte .
Le foie absorbe une partie du glucose du sang dans la veine porte provenant des intestins. Une fois que le foie a reconstitué ses réserves de glycogène (qui ne représentent qu'environ 100 g de glycogène lorsqu'il est plein), une grande partie du reste du glucose est convertie en acides gras comme décrit ci-dessous. Ces acides gras sont combinés avec du glycérol pour former des triglycérides qui sont conditionnés en gouttelettes très similaires aux chylomicrons, mais connus sous le nom de lipoprotéines de très basse densité (VLDL). Ces gouttelettes de VLDL sont manipulées exactement de la même manière que les chylomicrons, sauf que le reste de VLDL est connu sous le nom de lipoprotéine de densité intermédiaire (IDL), qui est capable d'éliminer le cholestérol du sang. Cela convertit l'IDL en lipoprotéines de basse densité (LDL), qui sont absorbées par les cellules qui ont besoin de cholestérol pour être incorporées dans leurs membranes cellulaires ou à des fins de synthèse (par exemple, la formation des hormones stéroïdes ). Le reste des LDL est éliminé par le foie.
Le tissu adipeux et les glandes mammaires en lactation absorbent également le glucose du sang pour le transformer en triglycérides. Cela se produit de la même manière que dans le foie, sauf que ces tissus ne libèrent pas les triglycérides ainsi produits sous forme de VLDL dans le sang. Les cellules du tissu adipeux stockent les triglycérides dans leurs gouttelettes de graisse, pour finalement les libérer à nouveau sous forme d'acides gras libres et de glycérol dans le sang (comme décrit ci - dessus ), lorsque la concentration plasmatique d'insuline est faible et que celle de glucagon et/ou d'épinéphrine est élevée . Les glandes mammaires déchargent la graisse (sous forme de gouttelettes de graisse de crème) dans le lait qu'elles produisent sous l'influence de la prolactine, une hormone hypophysaire antérieure .
Toutes les cellules du corps ont besoin de fabriquer et d'entretenir leurs membranes et les membranes de leurs organites. On ne sait pas s'ils dépendent entièrement des acides gras libres absorbés par le sang ou s'ils sont capables de synthétiser leurs propres acides gras à partir du glucose sanguin. Les cellules du système nerveux central auront presque certainement la capacité de fabriquer leurs propres acides gras, car ces molécules ne peuvent pas les atteindre à travers la barrière hémato-encéphalique , tandis que, d'autre part, aucune cellule du corps ne peut fabriquer les acides gras essentiels requis. acides qui doivent être obtenus à partir de l'alimentation et délivrés à chaque cellule via le sang.
Synthèse des acides gras
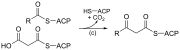
Tout comme la bêta-oxydation , la synthèse des acides gras à chaîne droite se produit via les six réactions récurrentes indiquées ci-dessous, jusqu'à ce que l'acide palmitique à 16 carbones soit produit.
Les schémas présentés montrent comment les acides gras sont synthétisés dans les microorganismes et répertorient les enzymes présentes dans Escherichia coli . Ces réactions sont réalisées par l'acide gras synthase II (FASII), qui contient en général plusieurs enzymes qui agissent comme un seul complexe. Le FASII est présent chez les procaryotes , les plantes, les champignons et les parasites, ainsi que dans les mitochondries .
Chez les animaux, ainsi que certains champignons tels que la levure, ces mêmes réactions se produisent sur l'acide gras synthase I (FASI), une grande protéine dimère qui possède toutes les activités enzymatiques nécessaires pour créer un acide gras. FASI est moins efficace que FASII ; cependant, il permet la formation de plus de molécules, y compris des acides gras « à chaîne moyenne » via une terminaison de chaîne précoce. Les enzymes, acyltransférases et transacylases, incorporent des acides gras dans des phospholipides, des triacylglycérols, etc. en transférant des acides gras entre un accepteur et un donneur d'acyle. Ils ont également pour mission de synthétiser les lipides bioactifs ainsi que leurs molécules précurseurs.
Une fois qu'un acide gras de carbone 16:0 a été formé, il peut subir un certain nombre de modifications, entraînant une désaturation et/ou un allongement. L'élongation, en commençant par le stéarate (18:0), est réalisée principalement dans le réticulum endoplasmique par plusieurs enzymes liées à la membrane. Les étapes enzymatiques impliquées dans le processus d'élongation sont principalement les mêmes que celles réalisées par la synthèse d'acides gras , mais les quatre principales étapes successives de l'élongation sont réalisées par des protéines individuelles, qui peuvent être physiquement associées.
| Étape | Enzyme | Réaction | La description |
|---|---|---|---|
| (une) | Acétyl CoA:ACP transacylase | Active l'acétyl CoA pour la réaction avec le malonyl-ACP | |
| (b) | Malonyl CoA:ACP transacylase |
|
Active le malonyl CoA pour la réaction avec l'acétyl-ACP |
| (c) | 3-cétoacyl-ACP synthase | Réagit à la chaîne acyle liée à l'ACP avec le malonyl-ACP à allongement de chaîne | |
| (ré) | 3-cétoacyl-ACP réductase | Réduit la cétone de carbone 3 en un groupe hydroxyle | |
| (e) | 3-Hydroxyacyl ACP déshydrase | Élimine l'eau | |
| (F) | Enoyl-ACP réductase | Réduit la double liaison C2-C3. |
Abréviations : ACP – Acyl carrier protein , CoA – Coenzyme A , NADP – Nicotinamide adénine dinucléotide phosphate .
Notez que lors de la synthèse des graisses, l'agent réducteur est le NADPH , tandis que le NAD est l'agent oxydant dans la bêta-oxydation (la décomposition des acides gras en acétyl-CoA). Cette différence illustre un principe général selon lequel le NADPH est consommé pendant les réactions de biosynthèse, tandis que le NADH est généré dans les réactions produisant de l'énergie. (Ainsi, le NADPH est également requis pour la synthèse du cholestérol à partir de l'acétyl-CoA, tandis que le NADH est généré pendant la glycolyse .) La source du NADPH est double. Lorsque le malate est décarboxylé par oxydation par le pyruvate "NADP + -linked malic enzyme" , du CO 2 et du NADPH sont formés. Le NADPH est également formé par la voie des pentoses phosphates qui convertit le glucose en ribose, qui peut être utilisé dans la synthèse de nucléotides et d'acides nucléiques , ou il peut être catabolisé en pyruvate.
Les produits finaux glycolytiques sont utilisés dans la conversion des glucides en acides gras
Chez l'homme, les acides gras sont formés à partir des glucides principalement dans le foie et le tissu adipeux , ainsi que dans les glandes mammaires pendant l'allaitement. Les cellules du système nerveux central fabriquent probablement aussi la plupart des acides gras nécessaires aux phospholipides de leurs membranes étendues à partir du glucose, car les acides gras transmis par le sang ne peuvent pas traverser la barrière hémato-encéphalique pour atteindre ces cellules. Cependant, comment les acides gras essentiels , que les mammifères ne peuvent pas synthétiser eux-mêmes, mais sont néanmoins des composants importants des membranes cellulaires (et d' autres fonctions décrites ci-dessus) les atteignent est inconnu.
Le pyruvate produit par la glycolyse est un intermédiaire important dans la conversion des glucides en acides gras et en cholestérol. Cela se produit via la conversion du pyruvate en acétyl-CoA dans la mitochondrie. Cependant, cet acétyl CoA doit être transporté dans le cytosol où se produit la synthèse des acides gras et du cholestérol. Cela ne peut pas se produire directement. Pour obtenir l'acétyl-CoA cytosolique, le citrate (produit par la condensation de l'acétyl CoA avec l'oxaloacétate) est retiré du cycle de l'acide citrique et transporté à travers la membrane mitochondriale interne dans le cytosol. Là, il est clivé par l' ATP citrate lyase en acétyl-CoA et oxaloacétate. L'oxaloacétate est renvoyé à la mitochondrie sous forme de malate (puis reconverti en oxaloacétate pour transférer plus d'acétyl-CoA hors de la mitochondrie). L'acétyl-CoA cytosolique est carboxylé par l' acétyl CoA carboxylase en malonyl CoA , la première étape engagée dans la synthèse des acides gras.
Régulation de la synthèse des acides gras
L'acétyl-CoA est transformé en malonyl-CoA par l' acétyl-CoA carboxylase , auquel cas le malonyl-CoA est destiné à alimenter la voie de synthèse des acides gras. L'acétyl-CoA carboxylase est le point de régulation de la synthèse des acides gras saturés à chaîne droite et est soumise à la fois à la phosphorylation et à la régulation allostérique . La régulation par phosphorylation se produit principalement chez les mammifères, tandis que la régulation allostérique se produit dans la plupart des organismes. Le contrôle allostérique se produit sous la forme d'une rétro-inhibition par le palmitoyl-CoA et d'une activation par le citrate. Lorsqu'il y a des niveaux élevés de palmitoyl-CoA, le produit final de la synthèse des acides gras saturés, il inactive allostériquement l'acétyl-CoA carboxylase pour empêcher une accumulation d'acides gras dans les cellules. Le citrate agit pour activer l'acétyl-CoA carboxylase à des niveaux élevés, car des niveaux élevés indiquent qu'il y a suffisamment d'acétyl-CoA pour alimenter le cycle de Krebs et produire de l'énergie.
Des taux plasmatiques élevés d' insuline dans le plasma sanguin (par exemple après les repas) provoquent la déphosphorylation et l'activation de l'acétyl-CoA carboxylase, favorisant ainsi la formation de malonyl-CoA à partir de l'acétyl-CoA, et par conséquent la conversion des glucides en acides gras, tandis que l' épinéphrine et le glucagon (libéré dans le sang pendant la famine et l'exercice) provoquent la phosphorylation de cette enzyme, inhibant la lipogenèse en faveur de l'oxydation des acides gras via la bêta-oxydation .
Troubles
Les troubles du métabolisme des acides gras peuvent être décrits en termes, par exemple, d' hypertriglycéridémie (taux trop élevé de triglycérides ) ou d'autres types d' hyperlipidémie . Ceux-ci peuvent être familiaux ou acquis.
Les types familiaux de troubles du métabolisme des acides gras sont généralement classés comme des erreurs innées du métabolisme des lipides . Ces troubles peuvent être décrits comme des troubles de l'oxydation des acides gras ou des troubles du stockage des lipides , et sont l'une des nombreuses erreurs innées du métabolisme qui résultent de défauts enzymatiques affectant la capacité du corps à oxyder les acides gras afin de produire de l'énergie dans les muscles, foie et d'autres types de cellules .
De plus, les cellules cancéreuses peuvent présenter un métabolisme irrégulier des acides gras en ce qui concerne à la fois la synthèse des acides gras et l'oxydation des acides gras mitochondriaux (FAO) qui sont impliquées dans divers aspects de la tumorigenèse et de la croissance cellulaire.